Lapisan Valencia
- 4589
- 1118
- Dewey Runolfsdottir
 Lapisan Valencia adalah tempat reaksi kimia terjadi
Lapisan Valencia adalah tempat reaksi kimia terjadi Apa lapisan Valencia?
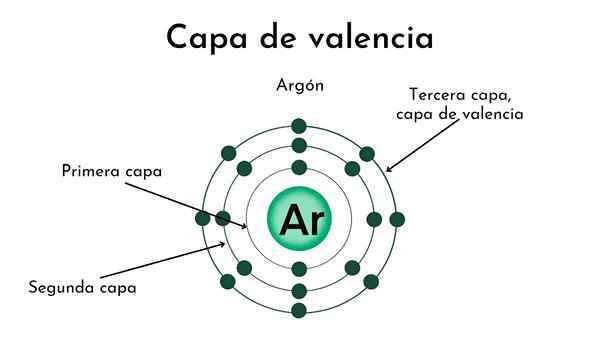
Itu Lapisan Valencia Itu adalah yang elektronnya bertanggung jawab atas sifat kimia dari suatu elemen. Elektron dalam lapisan ini berinteraksi dengan atom tetangga, untuk membentuk ikatan kovalen (A-B); Dan jika mereka beremigrasi dari satu atom ke atom lain yang lebih elektronegatif, tautan ionik (A+B-).
Lapisan ini ditentukan oleh nomor kuantum utama N, yang pada gilirannya menunjukkan periode di mana elemen berada di tabel periodik. Sedangkan pemesanan oleh kelompok tergantung pada jumlah elektron yang mengorbit di lapisan Valencia.
Sehingga untuk a N sama dengan 2, Anda dapat menempati delapan elektron: delapan kelompok (1-8).
 Inti atom dengan empat lapisan. Sumber: Gabriel Bolívar
Inti atom dengan empat lapisan. Sumber: Gabriel Bolívar Di gambar atas dan penutup arti lapisan valencia diilustrasikan. Titik hitam di tengah atom adalah nukleus, sedangkan lingkaran konsentris yang tersisa adalah lapisan elektronik yang ditentukan oleh N.
Berapa banyak lapisan yang dimiliki atom ini? Masing -masing memiliki warnanya sendiri, dan ketika ada empat, maka atom memiliki empat lapisan (N= 4).
Perhatikan bahwa warnanya merendahkan karena jarak dari lapisan meningkat ke nukleus. Lapisan Valencia adalah yang lebih jauh dari nukleus: warna yang paling jelas.
Apa lapisan Valencia?
Menurut gambar, lapisan Valencia tidak lebih dari orbital terakhir dari atom yang ditempati oleh elektron. Di lapisan biru muda, untuk N= 4 Ada serangkaian orbital 4S, 4P, 4D dan 4F; yaitu, di dalamnya ada sub -perusahaan lain dengan kemampuan elektronik yang berbeda.
Atom membutuhkan elektron untuk mengisi semua orbital 4n. Proses ini dapat diamati dalam konfigurasi elektronik elemen selama suatu periode.
Dapat melayani Anda: alkana linier: struktur, sifat, nomenklatur, contohMisalnya, kalium memiliki konfigurasi elektronik [AR] 4S1, Sedangkan kalsium, di sebelah kanan Anda, [ar] 4s2.
Menurut konfigurasi ini, apa lapisan Valencia? Istilah [AR] mengacu pada konfigurasi elektronik gas Noble Argon 1s22s22 p63S23p6. Ini mewakili lapisan dalam atau tertutup (yang juga dikenal sebagai Inti).
Karena orbital 4S adalah yang memiliki energi terbesar, dan di mana elektron baru masuk, itu mewakili lapisan valensi untuk K dan CA. Jika atom K dan CA dibandingkan dengan gambar, [ar] akan menjadi semua lapisan dalam biru; dan 4s lapisan biru muda, eksternal.
Karakteristik Lapisan Valencia
Dari atas, beberapa karakteristik lapisan Valencia dapat diringkas untuk semua atom:
-Tingkat energinya lebih tinggi; Apa yang sama, lebih menarik dari nukleus dan memiliki kepadatan elektronik terendah (dibandingkan dengan lapisan lain).
-Itu tidak lengkap. Oleh karena itu, itu akan terus diisi dengan elektron sebagai periode dari kiri ke kanan sedang bepergian di tabel periodik.
-Campur tangan dalam pembentukan tautan kovalen atau ionik.
Dalam hal logam kalium dan kalsium, mereka teroksidasi untuk berubah menjadi kation. K+ Ini memiliki konfigurasi elektronik [AR], karena kehilangan hanya elektron eksternal 4S1. Dan di sisi CA2+, Konfigurasinya juga [ar]; Karena alih -alih kehilangan elektron, kehilangan dua (4s2).
Tapi apa perbedaan antara k+ dan ca2+, Jika keduanya kehilangan elektron lapisan valensi mereka dan memiliki konfigurasi elektronik [AR]? Perbedaannya ada pada radio ioniknya.
Dapat melayani Anda: Merkurius oksida (HG2O)Ac2+ lebih kecil dari k+ Karena atom kalsium memiliki proton tambahan yang menarik elektron eksternal (tertutup atau valencia) lebih banyak gaya).
Lapisan Valencia 4S belum hilang: hanya kosong untuk ion -ion ini.
Contoh Lapisan Valencia
Konsep lapisan Valencia dapat secara langsung atau tidak langsung dalam banyak aspek kimia.
Karena elektron mereka adalah yang berpartisipasi dalam pembentukan ikatan, topik apa pun yang membahasnya (TEV, RPECV, mekanisme reaksi, dll.) Anda harus merujuk pada lapisan tersebut.
Ini karena, lebih penting daripada lapisan valensi, mereka adalah elektronnya, yang disebut elektron valencia. Saat mewakili konstruksi progresif konfigurasi elektronik, mereka menentukan struktur elektronik atom, dan, oleh karena itu, sifat kimianya.
Dari informasi ini dari satu atom A dan B lainnya, struktur senyawa mereka dapat dimasukkan melalui struktur Lewis. Demikian juga, struktur elektronik dan molekul dari berbagai senyawa dapat ditentukan berkat jumlah elektron valensi.
Contoh -contoh yang mungkin dan paling sederhana dari lapisan valensi berada dalam tabel periodik; Secara khusus, dalam konfigurasi elektronik.
Contoh 1
Dimungkinkan untuk mengidentifikasi elemen dan lokasinya di tabel periodik hanya dengan konfigurasi elektronik. Jadi, jika suatu elemen x memiliki konfigurasi [kr] 5s25 p1, Tentang apa dan periode dan kelompok apa?
Mengingat N= 5, x berada di periode kelima. Selain itu, ia memiliki tiga elektron Valencia: dua dalam orbital 5S2 Dan satu dari 5p1. Lapisan Dalam [KR] tidak memberikan informasi lebih lanjut.
Ini dapat melayani Anda: Asam Bromydric (HBR)Karena X memiliki tiga elektron, dan orbital 5P -nya tidak lengkap, ia berada di blok P; Selain itu, dalam kelompok IIIA (Romawi) atau 13 (sistem penomoran saat ini oleh IUPAC). X kemudian menjadi elemen India, masuk.
Contoh 2
Apa elemen x dengan konfigurasi elektronik [kr] 4d105S1? Perhatikan bahwa seperti di, itu milik periode 5, karena orbital 5s1 adalah energi terbanyak. Namun, lapisan Valencia juga mencakup orbital 4D, karena itu tidak lengkap.
Lapisan Valencia kemudian dapat ditetapkan sebagai NSNP, untuk elemen blok P atau S; atau (n-1) DNS, untuk elemen blok D. Sehingga elemen misterius X milik Blok D karena konfigurasi elektroniknya adalah tipe (N-1) DNS (4D105S1).
Kelompok mana yang berasal? Menambahkan sepuluh elektron orbital 4D10, dan salah satu dari 5s1, X memiliki sebelas elektron dari Valencia. Oleh karena itu, harus berlokasi di Grup IB U 11. Kemudian bepergian melalui periode 5 dari tabel periodik hingga kelompok 11 Anda mencapai elemen perak, AG.
Referensi
- Shiver & Atkins. (2008). Kimia Anorganik (Edisi Keempat, hlm. 23). MC Graw Hill.
- Whitten, Davis, Peck & Stanley. Kimia (ed ke -8.). Pembelajaran Cengage, P. 287.
- NDT Resource Center (S.F.). Shell valensi. Diambil dari: nde-ed.org
- Clackamas Community College (2002). Elektron valensi. Diperoleh dari: DL.Clackamas.Edu
- Libretteks kimia (s.F.). Valensi dan elektron inti. Pulih dari: chem.Librettexts.org

