Asam asetat (CH3COOH)
- 3233
- 17
- Dewey Runolfsdottir
 Asam asetat bertanggung jawab atas rasa dan bau cuka yang khas
Asam asetat bertanggung jawab atas rasa dan bau cuka yang khas Apa itu asam asetat?
Dia asam asetat, O Asam Estanoat, ini adalah cairan organik yang tidak berwarna yang formula kimianya adalah Cho3Cooh. Ini hadir dalam cuka, yang memberikan bau dan rasanya yang khas. Cuka adalah larutan asam asetat berair dengan konsentrasi 5%, kira -kira.
Seperti namanya, itu adalah senyawa asam, dan oleh karena itu, cuka memiliki nilai pH kurang dari 7. Di hadapan garam asetatnya merupakan sistem redaman yang efektif dalam regulasi pH antara 2,76 dan 6,76, yaitu, mempertahankan pH dalam interval tersebut terhadap penambahan basa atau asam sedang atau asam.
Setelah asam format, hcooh, adalah salah satu asam organik paling sederhana, yang juga mewakili titik akhir dari banyak proses fermentasi. Ini biasanya digunakan untuk mendandani makanan dan juga untuk menghilangkan kotoran dan mikroorganisme dari sayuran.
Sejarah
Manusia telah menggunakan fermentasi banyak buah, kacang -kacangan, sereal, dll., Untuk mendapatkan minuman beralkohol, produk transformasi gula, seperti glukosa, dalam etanol, ch3Ch2Oh.
Mungkin karena metode awal untuk produksi alkohol dan cuka adalah fermentasi, mungkin mencoba menghasilkan alkohol pada saat yang tidak pasti, berabad -abad yang lalu, cuka diperoleh secara tidak sengaja.
Sudah di abad ketiga.C., Filsuf Yunani Theophastus menggambarkan tindakan cuka pada logam untuk produksi pigmen, seperti timah putih.
1800
Pada tahun 1823, peralatan berbentuk menara dirancang di Jerman untuk fermentasi aerobik dari berbagai produk, untuk mendapatkan asam asetat dalam bentuk cuka.
Pada tahun 1846, Herman Foelbe dicapai untuk pertama kalinya sintesis asam asetat melalui penggunaan senyawa anorganik. Sintesis dimulai dengan klorinasi karbon disulfida dan menyimpulkan, setelah dua reaksi, dengan reduksi elektrolitik menjadi asam asetat.
Pada akhir abad ke -19 dan awal kedua puluh, karena jj. Weizmann mulai menggunakan bakteri Clostridium acetobutylicum Untuk produksi asam asetat, melalui fermentasi anaerob.
Itu dapat melayani Anda: hubungan kimia dan teknologi dengan manusia, kesehatan dan lingkungan1900
Pada awal abad ke -20, teknologi dominan adalah produksi asam asetat dengan oksidasi asetaldehida.
Pada tahun 1925, Henry Dreyfus, dari perusahaan Inggris Celanese, merancang pabrik percontohan untuk karbonilasi metanol. Selanjutnya, pada tahun 1963, perusahaan Jerman BASF memperkenalkan penggunaan kobalt sebagai katalisator.
Otto Hromatka dan Heinrich Ebner (1949), merancang tangki dengan sistem agitasi dan pasokan udara untuk fermentasi aerobik, dimaksudkan untuk produksi cuka. Implement ini, dengan beberapa adaptasi, tetap digunakan.
Pada tahun 1970, perusahaan Amerika Utara Monsanto menggunakan sistem katalis berdasarkan rhodium untuk metanol karbonilasi.
Selanjutnya, perusahaan BP pada tahun 1990, memperkenalkan prosedur CATIVA dengan menggunakan katalis Iridium untuk tujuan yang sama. Metode ini ternyata lebih efisien dan kurang agresif lingkungan daripada metode Monsanto.
Struktur asam asetat
 Struktur Asam Asetat Kimia
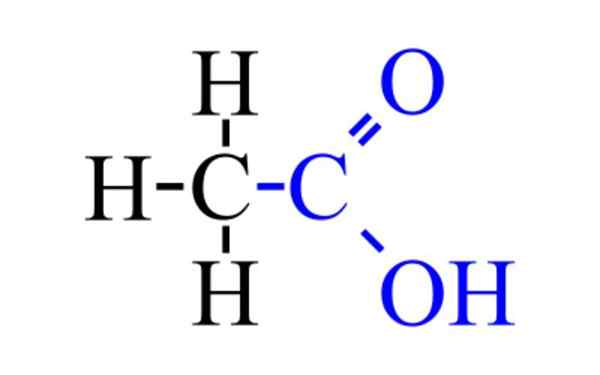
Struktur Asam Asetat Kimia Gambar atas menunjukkan struktur asam asetat yang diwakili dengan model bola dan batang. Bola merah sesuai dengan atom oksigen, yang pada gilirannya milik kelompok karboksil, -cooh. Oleh karena itu, itu adalah asam karboksilat. Di sisi kanan struktur Anda memiliki kelompok metil, -ch3.
Seperti yang dapat dilihat, ini adalah molekul yang sangat kecil dan sederhana. Ini memiliki momen dipol permanen karena kelompok -COOH, yang juga memungkinkan asam asetat membentuk dua jembatan hidrogen berturut -turut.
Jembatan inilah yang secara spasial memandu molekul CH3COOH untuk membentuk karunia dalam keadaan cair (dan gas).
 Dua jembatan hidrogen
Dua jembatan hidrogen Naik pada gambar diamati bagaimana kedua molekul diatur untuk membentuk dua jembatan hidrogen: O-H-O dan O-H-O.
Untuk menguapkan asam asetat, energi yang cukup harus dipasok untuk memecahkan interaksi ini, itulah sebabnya cairan dengan titik didih lebih besar dari air (sekitar 118 ° C).
Sifat fisik dan kimia asam asetat
Nama Kimia
Asam:
Dapat melayani Anda: aluminium bromida- Asetat
- Etanoik
- Etil
Formula molekul
C2H4SALAH SATU2 atau ch3Cooh.
Penampilan fisik
Cairan tidak berwarna.
Bau
Acre Karakteristik.
Rasa
Membakar.
Titik didih
244 ºF pada 760 mmHg (117,9 ºC).
Titik lebur
61.9 ºF (16.6 ºC).
titik pengapian
112 ºF (kaca terbuka) 104 ºF (kaca tertutup).
Kelarutan air
106 mg/ml pada 25 ºC (ini dapat larut dalam semua proporsi).
Kelarutan dalam pelarut organik
Itu larut dalam etanol, etil eter, aseton dan benzena. Itu juga larut dalam karbon tetrachloride.
Kepadatan
1.051 g/cm3 pada 68 ºF (1.044 g/cm3 pada 25 ºC).
Kepadatan uap
2.07 (dengan relasi udara = 1).
Tekanan uap
15,7 mmHg pada 25 ºC.
Penguraian
Saat dipanaskan hingga lebih dari 440 ºC, ia rusak untuk menghasilkan karbon dioksida dan metana.
Zat yang lengket dan kental
1.056 mpascal pada 25 ° C.
Korosivitas
Asam asetat glasial sangat korosif dan konsumsi dapat menyebabkan lesi kerongkongan dan pylorus parah pada manusia.
Panas pembakaran
874.2 kJ/mol.
Panas penguapan
23,70 kJ/mol pada 117,9 ºC.
23,36 kJ/mol pada 25,0 ºC.
ph
- Larutan konsentrasi 1 m memiliki pH 2.4.
- Untuk solusi 0,1m, pHnya adalah 2,9.
- Dan 3,4 jika solusinya 0,01m.
Tegangan permukaan
27,10 mn/m a 25 ºC.
PKA
4.76 hingga 25 ºC.
Reaksi kimia
Asam asetat bersifat korosif untuk banyak logam, melepaskan gas h2 dan membentuk garam logam yang disebut asetat. Dengan pengecualian kromium asetat (II), asetat larut dalam air.
Reaksinya dengan magnesium diwakili dengan persamaan kimia berikut:
Mg (s) +2 cho3Cooh (ag) => (ch3Mendekut)2Mg (ag) +h2 (G)
Dengan reduksi, asam asetat membentuk etanol. Anda juga dapat membentuk anhidrida asetat karena kehilangan air dari dua molekul air.
Penggunaan asam asetat
Industrialis
- Asam asetat bereaksi dengan etilen dengan adanya oksigen untuk membentuk monomer vinil asetat, menggunakan paladium sebagai katalis untuk reaksi. Polymeriza vinyl asetat dalam polivinil asetat, yang digunakan sebagai komponen lukisan dan bahan perekat.
- Bereaksi dengan alkohol yang berbeda untuk produksi ester, termasuk etil asetat dan propil asetat. Ester asetat digunakan sebagai pelarut tinta, nitroselulosa, pelapis, pernis dan lacas akrilik.
Dapat melayani Anda: paduan- Dengan kondensasi dua molekul asam asetat, anhidrida asetat terbentuk, CH3Co-o-coch3. Senyawa ini mengintervensi dalam sintesis selulosa asetat, polimer yang merupakan kain sintetis dan digunakan dalam elaborasi film fotografi.
Sebagai pelarut
- Ini adalah pelarut polar yang mampu melarutkan senyawa polar seperti garam dan gula anorganik, tetapi juga melarutkan senyawa non -polar, seperti minyak dan lemak. Selain itu, asam asetat larut dengan pelarut polar dan non -polar.
- Ketidakcocokan asam asetat dalam alkana tergantung pada perpanjangan rantai ini: karena panjang string alkana meningkat, keliru dengan asam asetat berkurang.
Dokter
- Asam asetat yang diencerkan digunakan sebagai antiseptik, diterapkan secara topikal, dengan kemampuan untuk menyerang bakteri seperti streptokokus, staphylococci dan pseudomonas. Karena tindakan ini digunakan dalam pengobatan infeksi kulit.
- Ini digunakan dalam endoskopi esofagus Barrett, suatu kondisi di mana lapisan kerongkongan dimodifikasi, menjadi mirip dengan celah usus kecil.
- Gel asam asetat 3% tampaknya menjadi adjuvan yang efektif untuk perawatan dengan obat misoprostol vagina, menginduksi aborsi medis pada kuartal tengah, terutama pada wanita dengan pH vagina 5 atau lebih.
- Ini digunakan sebagai pengganti pengelupasan kimia. Namun, komplikasi dengan penggunaan ini telah muncul, karena telah dilaporkan, setidaknya, kasus luka bakar yang diderita oleh pasien.
- Ini digunakan sebagai pewarna untuk mendeteksi papillomavirus manusia (HPV).
Dalam makanan
Cuka telah digunakan sebagai bumbu dan penyedap makanan selama berabad -abad, jadi ini adalah aplikasi asam asetat yang paling terkenal.
Referensi
- Apa itu asam etanoat? Pulih dari byjus.com
- ASAM ASETAT. Pulih dari pubchem.NCBI.Nlm.Nih.Pemerintah
- Glasial asam asetat. Dipulihkan dari Chemicalbook.com

