Konsentrasi Kimia

- 1753
- 348
- Ernesto Mueller
 Konsentrasi kimia adalah apa yang menentukan proporsi zat terlarut dan pelarut dalam larutan kimia
Konsentrasi kimia adalah apa yang menentukan proporsi zat terlarut dan pelarut dalam larutan kimia Apa itu konsentrasi kimia?
Itu Konsentrasi Kimia Ini adalah properti dari solusi yang mewakili jumlah zat terlarut untuk setiap unit solusi. Dengan kata lain, itu adalah angka yang menunjukkan proporsi di mana zat terlarut dan pelarut berada.
Ingatlah bahwa larutan adalah campuran homogen yang dibentuk oleh pelarut (umumnya cair) dan satu atau lebih zat yang dilarutkan dalam pelarut yang kita sebut zat terlarut. Solusi ditandai oleh pelarut, zat terlarut dan konsentrasi.
Konsentrasi adalah properti properti yang sangat berguna, karena memungkinkan kami untuk menggambarkannya. Misalnya, jika kita tahu bahwa konsentrasi garam dalam air laut adalah 35 gram untuk setiap liter, maka kita tahu bahwa, di rumah kita kita melarutkan 35 gram garam dalam satu liter larutan, kita akan mendapatkan solusi asin yang sama dengan air laut yang sama.
Karakteristik konsentrasi kimia
Itu adalah properti yang intensif
Ini adalah karakteristik utama konsentrasi. Intensif berarti tidak tergantung pada jumlah solusi yang kami miliki. Sebagai contoh, ini berarti bahwa konsentrasinya sama dalam setetes air laut daripada 100 liter yang sama.
Dapat bervariasi dengan suhu
Secara umum, cairan memperluas atau meningkatkan volumenya saat pemanasan. Ini juga berlaku untuk solusi. Untuk alasan ini, konsentrasi yang diekspresikan tergantung pada volume dapat sedikit berubah saat memanaskan atau mendinginkan larutan.
Ini dapat mencakup rentang jangkauan yang sangat luas
Terlepas dari unit di mana konsentrasi kimia diekspresikan, ia dapat memiliki dari nilai yang relatif besar, ke nilai yang sangat kecil.
Misalnya, konsentrasi larutan yang dinyatakan dalam persentase dapat memiliki nilai dari 0% hingga 100%, sehingga mencakup banyak urutan besarnya. Kami bisa menyiapkan solusi 90%, karena kami juga bisa menyiapkan satu dengan 10-12%, yang hampir 14 urutan besarnya kecil.
Untuk apa konsentrasi kimia?
Mengetahui konsentrasi suatu larutan memungkinkan kita untuk menggambarkannya. Ada banyak sifat solusi yang bergantung pada konsentrasinya. Misalnya, titik pencairan dan didih tergantung pada konsentrasi, jadi mengetahui hal itu memungkinkan kita untuk menghitung kedua sifat ini.
Dapat melayani Anda: keadaan vitreousDi sisi lain, konsentrasi memungkinkan kita untuk dengan mudah membandingkan solusi dengan yang lain. Jika kita memiliki dua solusi air dengan gula, mengetahui konsentrasi mereka akan memungkinkan kita untuk mengetahui mana dari keduanya yang lebih manis.
Selain itu, semua reaksi kimia yang memungkinkan kehidupan sangat bergantung pada konsentrasi zat terlarut yang tak ada habisnya dalam sel dan lingkungan makhluk hidup.
Misalnya, konsentrasi oksigen di udara menentukan apakah seseorang akan mati lemas atau tidak; PH larutan (yang merupakan cara untuk mengukur konsentrasi ion H+) Tentukan apakah bakteri akan hidup dan bereproduksi atau jika, sebaliknya, itu akan mati; dan konsentrasi racun akan menentukan apakah itu akan mematikan atau tidak.
Jenis unit konsentrasi
Konsentrasi larutan adalah satu, jadi tidak benar untuk berbicara tentang jenis konsentrasi. Namun, konsentrasi yang sama dapat diekspresikan dalam berbagai jenis unit konsentrasi. Ini adalah:
- Unit konsentrasi fisik
- Unit Konsentrasi Kimia
Unit konsentrasi fisik
Ini ditandai dengan mengekspresikan jumlah zat terlarut dan pelarut baik dalam satuan massa atau volume. Mereka disebut unit fisik, karena mereka dikaitkan dengan massa dan volume, bukan tahi lalat dan setara.
Ketika kami membandingkan dua solusi yang memiliki konsentrasi fisik yang sama, kami tidak dapat memastikan bahwa mereka memiliki jumlah atom dan molekul yang sama. Inilah yang membedakannya dari unit konsentrasi kimia.
Unit fisik konsentrasi yang paling umum adalah:
- Judul Sederhana (TS)
- %berat/berat (%p/p) atau massa/massa (%m/m)
- %berat/volume (%p/v) atau massa/volume (%m/v)
- % volume/volume (% v/v)
- Bagian per juta berat/berat (ppmp/p) atau massa/massa (ppmm/m)
- Bagian per juta berat/volume (ppmp/v) atau massa/volume (ppmm/v)
- Bagian per juta volume/volume (ppmV/v)
Unit Konsentrasi Kimia
Dalam kasus unit kimia, jumlah zat terlarut dan, dalam beberapa kasus, bahwa pelarut atau larutan, dinyatakan dalam jumlah partikel atau tahi lalat atau setara yang ada dalam larutan.
Mereka disebut unit kimia, karena dua solusi yang memiliki konsentrasi kimia yang sama memang memiliki jumlah atom, molekul atau ion zat terlarut yang setara per unit larutan, seperti yang mungkin terjadi.
Dapat melayani Anda: Peraturan Kelarutan: Aspek dan Aturan UmumUnit kimia yang paling umum adalah:
- Molaritas (M)
- Molalitas (M)
- Fraksi molar (x)
- Normalitas (n)
Formula unit konsentrasi fisik
Judul Sederhana (TS)
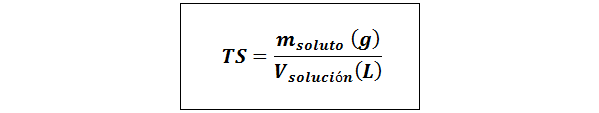
Dimana mterlarut mewakili massa zat terlarut dalam gram dan vlarutan Itu adalah volume solusi dalam liter.
%berat/berat (%p/p) atau massa/massa (%m/m)
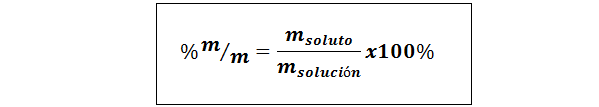
Dimana mterlarut dan mlarutan masing -masing mewakili massa zat terlarut dan solusinya. Unit massa apa pun dapat digunakan (G, MG, KG, dll.), selama kedua massa dinyatakan dalam unit yang sama.
%berat/volume (%p/v) atau massa/volume (%m/v)
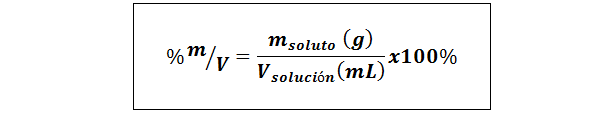
Dimana mterlarut Itu adalah massa solusi dalam gram dan vlarutan Ini adalah volume solusi, dalam hal ini dalam mililiter.
% volume/volume (% v/v)

Dimana vterlarut dan vlarutan masing -masing mewakili volume zat terlarut dan solusinya. Dalam hal ini, unit apa pun dapat digunakan untuk mengekspresikan volume ini, asalkan sama untuk keduanya.
Bagian per juta berat/berat (ppmp/p) atau massa/massa (ppmm/m)
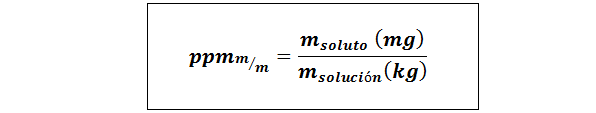
Dimana mterlarut dan mlarutan Mereka mewakili massa zat terlarut dan solusi dalam miligram dan kilogram masing -masing.
Bagian per juta berat/volume (ppmp/v) atau massa/volume (ppmm/v)
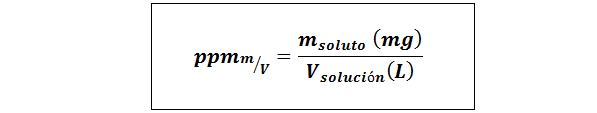
Dimana mterlarut Ini adalah massa solusi dalam miligram dan vlarutan Ini adalah volume solusi, dalam hal ini dalam liter.
Bagian per juta volume/volume (ppmV/v)
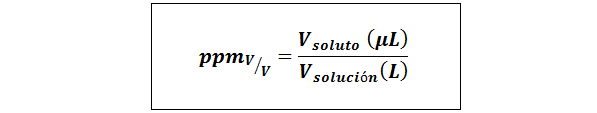
Dimana vterlarut dan vlarutan Mereka adalah volume zat terlarut dan solusi dalam mikroliter dan liter, masing -masing.
Rumus unit konsentrasi kimia
Dalam kasus unit konsentrasi kimia, jumlah komponen larutan, khususnya zat terlarut, dinyatakan baik dalam jumlah mol atau dalam jumlah yang setara. Jumlah ini memiliki jumlah nyata partikel (atom, molekul atau ion, seperti kasusnya).
Jumlah ini tidak dapat diketahui hanya dengan menimbang atau mengukur volume zat, tetapi perlu untuk mengetahui komposisi atau formula kimia senyawa untuk menentukan konsentrasi. Inilah alasan utama mengapa mereka disebut konsentrasi kimia.
Selanjutnya, berbagai formula disajikan untuk menghitung empat konsentrasi kimia yang paling umum digunakan:
Molaritas (M)
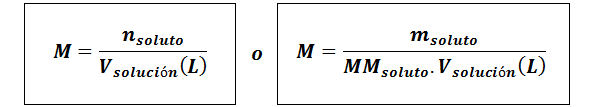
Di manaterlarut Mereka adalah mol zat terlarut, mterlarut mewakili massa zat terlarut dalam gram, mmterlarut adalah massa molar dan vlarutan Itu adalah volume solusi dalam liter.
Molalitas (M)
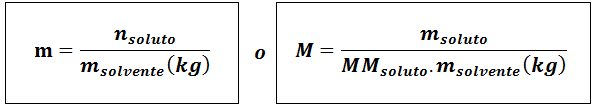
Di manaterlarut Mereka adalah mol zat terlarut, mterlarut mewakili massa zat terlarut dalam gram, mmterlarut Itu adalah massa molar dan mpelarut Itu adalah massa pelarut dalam kilogram.
Dapat melayani Anda: solvasiFraksi molar (x)
Fraksi molar dapat dihitung untuk zat terlarut dan pelarut. Fraksi molar zat terlarut adalah:
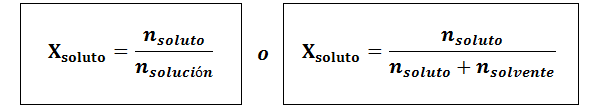
Pelarutnya adalah:
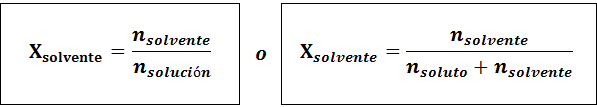
Hubungan antara kedua fraksi molar adalah:
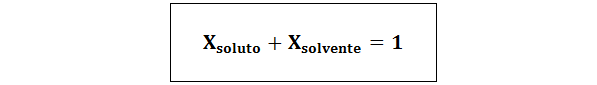
Dalam semua kasus nterlarut, Nlarutan dan Npelarut adalah mol zat terlarut, larutan dan pelarut masing -masing.
Normalitas (n)
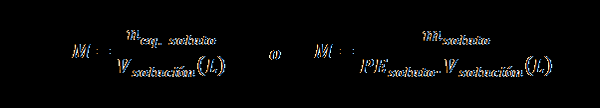
Di sini nPersamaan. terlarut mewakili jumlah yang setara dengan zat terlarut, mterlarut mewakili massa zat terlarut, PEterlarut Ini adalah bobot yang setara dari zat terlarut dan vlarutan Itu adalah volume solusi dalam liter.
Contoh konsentrasi kimia
- Konsentrasi garam dalam air laut adalah 35 g/L, yang sesuai dengan molaritas 0,60 mol/L.
- Konsentrasi gula darah rata -rata adalah antara 82 mg/dL dan 110 mg/dL. Konsentrasi ini setara dengan judul sederhana pada 0,82 g/L dan 1,10 g/L, dan dalam molaritas pada 4.4.10-3 mol/l dan 6.1.10-3 Mol/L, masing -masing.
- Udara dapat dianggap sebagai larutan gas yang dibentuk terutama oleh nitrogen dan oksigen, pelarutnya nitrogen, karena dalam proporsi yang lebih besar. Larutan gas ini mengandung fraksi oksigen dan nitrogen 0,22 sekitar 0,78.
- Baja adalah paduan antara besi dan karbon. Meskipun mereka bukan solusi yang ketat, ini adalah campuran padat homogen yang biasanya mengandung konsentrasi karbon dalam urutan 0,03% dan 1,075% dalam massa.
- Terlepas dari efeknya yang menghancurkan bagi lingkungan dan untuk kesehatan manusia, konsentrasi banyak polutan biasanya sangat rendah. Contohnya adalah konsentrasi maksimum logam beracun arsenik dalam air. Organisasi Kesehatan Dunia (WHO) menetapkan bahwa air minum tidak boleh mengandung konsentrasi arsenik lebih besar dari 10ppb m/v (bagian per miliar atau nanogram per liter). Konsentrasi ini setara dengan 0.010 ppm m/v.
Referensi
- BBC (s. F.). Konsentrasi Solusi - Perhitungan dalam Kimia - AQA - Tinjauan Kimia GCSE (Ilmu Tunggal) - AQA. BBC diambil.bersama.Inggris.
- Inilah arti konsentrasi dalam kimia (2020). Diambil dari Thoughtco.com.
- Librettexts (2022). 4.5: Konsentrasi Solusi. Diambil dari Chem.Librettexts.org.
- Mandal, a., Md. (2021). Nilai gula darah normal. Diambil dari berita-medis.bersih.
- Bahan kimia.Net (s. F.). Konsentrasi Kimia. Diambil dari bahan kimia.bersih.

