Tahap fosforilasi oksidatif, fungsi dan inhibitor
- 4585
- 1478
- Ray Thiel
Itu fosforilasi oksidatif Ini adalah proses di mana molekul ATP disintesis dari ADP dan Pyo (Fosfat anorganik). Mekanisme ini dilakukan oleh bakteri dan sel eukariotik. Dalam sel eukariotik, fosforilasi dilakukan dalam matriks mitokondria sel non -fotosintetik.
Produksi ATP diarahkan oleh transfer elektron dari koenzim NADH atau FADH2 juga2. Proses ini mewakili produksi energi terbesar dalam sel dan berasal dari degradasi karbohidrat dan lemak.
 Sumber: Robot8a [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)]
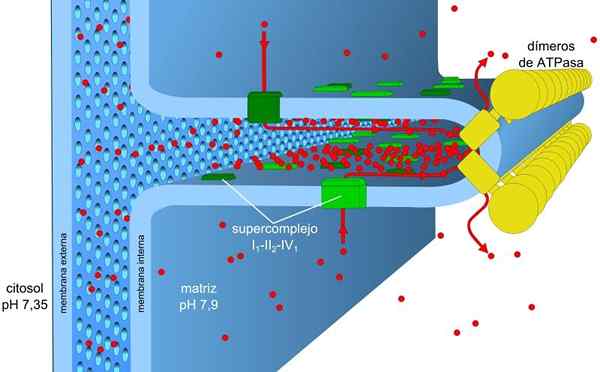
Sumber: Robot8a [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)] Energi yang disimpan dalam gradien beban dan pH, juga dikenal sebagai gaya motor protonik, memungkinkan proses ini dilakukan. Gradien proton yang dihasilkan, menyebabkan bagian eksternal membran memiliki beban positif karena konsentrasi proton (h+) dan matriks mitokondria negatif.
[TOC]
Di mana fosforilasi oksidatif terjadi?
Transportasi elektron dan proses fosforilasi oksidatif dikaitkan dengan membran. Dalam prokariota mekanisme ini dilakukan melalui membran plasma. Dalam sel eukariotik mereka terkait dengan membran mitokondria.
Jumlah mitokondria yang ditemukan dalam sel bervariasi sesuai dengan jenis sel. Misalnya, pada mamalia eritrosit tidak memiliki organel ini, sedangkan tipe sel lainnya, seperti sel otot, dapat memiliki jutaan dari mereka.
Membran mitokondria terdiri dari membran eksternal sederhana, membran internal yang agak lebih kompleks, dan di tengah -tengah ruang intermembran, di mana banyak enzim yang bergantung pada ATP berada.
Membran luar mengandung protein yang disebut porina yang membentuk saluran untuk difusi sederhana molekul kecil. Membran ini bertanggung jawab untuk mempertahankan struktur dan bentuk mitokondria.
Membran internal memiliki kepadatan yang lebih besar dan kaya akan protein. Ini juga tahan air untuk molekul dan ion sehingga, untuk melintasi, mereka membutuhkan protein intermembranal yang mengangkutnya.
Di dalam matriks, lipatan membran internal memanjang, membentuk punggung yang memungkinkannya memiliki area yang luas dalam volume kecil.
Pusat energi sel
Mitokondria dianggap sebagai pusat energi seluler. Di dalamnya adalah enzim yang terlibat dalam proses siklus asam sirat, oksidasi asam lemak dan enzim redoks dan protein transportasi elektron dan fosforilasi PhD.
Gradien konsentrasi proton (gradien pH) dan gradien beban atau potensi listrik di membran internal mitokondria, adalah penyebab gaya motorik prottonik. Permeabilitas kecil dari membran internal untuk ion (selain h+) memungkinkan mitokondria memiliki gradien tegangan yang stabil.
Transportasi elektronik, proton pemompaan dan ATP memperoleh secara bersamaan di mitokondria, berkat gaya motor protonik. Gradien pH mempertahankan kondisi asam dalam matriks intermembran dan mitokondria dengan kondisi alkali.
Untuk setiap dua elektron yang ditransfer ke O2 Sekitar 10 proton dipompa oleh membran, menciptakan gradien elektrokimia. Energi yang terlepas dalam proses ini diproduksi secara bertahap dengan melewati elektron melalui rantai konveyor.
Tahapan
Energi yang dilepaskan selama reaksi reduksi oksida NADH dan FADH2 Ini sangat tinggi (sekitar 53 kkal/mol untuk setiap pasangan elektron), sehingga digunakan dalam pembuatan molekul ATP, harus secara bertahap diproduksi dengan lewatnya elektron melalui transporter.
Ini diselenggarakan di empat kompleks yang terletak di membran mitokondria internal. Kopling reaksi ini terhadap sintesis ATP dilakukan di kompleks kelima.
Dapat melayani Anda: B Limfosit: Karakteristik, Struktur, Fungsi, JenisRantai transportasi elektron
NADH mentransfer beberapa elektron yang memasuki kompleks I rantai transportasi elektron. Elektron dipindahkan ke mononukleotida flavina, dan kemudian ke ubiquinone (koenzim Q) melalui konveyor gula-gula. Proses ini melepaskan sejumlah besar energi (16,6 kkal/mol).
Ubiquinona mengangkut elektron melalui membran ke kompleks III. Di kompleks ini elektron melewati sitokrom B dan C1 Terima kasih kepada transporter gula-gula.
Dari kompleks III, elektron dilewati ke kompleks IV (sitokrom C oksidase), ditransfer satu dengan sitokrom C (protein membran perifer). Di kompleks IV elektron melewati sepasang ion tembaga (Cuke2+), lalu ke sitokrom cke, Kemudian ke sepasang ion tembaga lainnya (CuB2+) dan dari ini ke sitokrom ke3.
Akhirnya, elektron dipindahkan ke O2 yang merupakan akseptor terakhir dan membentuk molekul air (h2O) untuk setiap pasangan elektron yang diterima. Bagian elektron dari kompleks IV ke O2 Ini juga menghasilkan banyak energi bebas (25,8 kkal/mol).
Succinato CoQ reduktase
Kompleks II (CoQ reductase suksinat) menerima sepasang elektron dari siklus asam sitrat, karena oksidasi molekul suksinat menjadi fumarate. Elektron ini ditransfer ke FAD, kemudian melewati kelompok besi-Azufre, ke Ubiquinona. Dari koenzim ini mereka pergi ke kompleks III dan mengikuti rute yang dijelaskan sebelumnya.
Energi yang dilepaskan dalam reaksi transfer elektron ke FAD tidak cukup untuk meningkatkan proton melalui membran, sehingga pada langkah rantai ini tidak ada kekuatan motorik prottonik, dan akibatnya fadh menghasilkan lebih sedikit h+ dari Nadh.
Penggabungan atau transduksi energi
Energi yang dihasilkan dalam proses transportasi elektron yang dijelaskan sebelumnya, harus digunakan untuk produksi ATP, reaksi yang dikatalisis oleh ATP sintase atau enzim kompleks V. Konservasi energi semacam itu dikenal sebagai penggabungan energi, dan mekanismenya sulit untuk mengkarakterisasi.
Beberapa hipotesis telah dijelaskan untuk menggambarkan transduksi energi ini. Yang paling diterima adalah hipotesis kopling chemosmotic, yang dijelaskan di bawah ini.
Kopling chemosmotic
Mekanisme ini mengusulkan bahwa energi yang digunakan untuk sintesis ATP berasal dari gradien protonik dalam membran sel. Proses ini mengintervensi mitokondria, kloroplas dan bakteri dan terkait dengan transportasi elektron.
Kompleks I dan IV transportasi elektronik bertindak sebagai pompa proton. Ini menderita perubahan konformasi yang memungkinkan mereka memompa proton ke ruang intermembranal. Di kompleks IV untuk setiap pasangan elektron, dua proton dipompa di luar membran dan dua lagi tetap dalam pembentukan matriks H2SALAH SATU.
Ubiquinona dalam kompleks III menerima proton kompleks I dan II dan membebaskannya di luar membran. Kompleks I dan III Masing -masing memungkinkan bagian dari empat proton untuk setiap pasangan elektron yang diangkut.
Matriks mitokondria memiliki konsentrasi proton yang rendah dan potensi listrik negatif sementara ruang intermembran menyajikan kondisi terbalik. Aliran proton melalui membran ini menyiratkan gradien elektrokimia yang menyimpan energi yang diperlukan (± 5 kkal/mol dengan proton) untuk sintesis ATP.
Sintesis ATP
Enzim ATP sintetase adalah kompleks kelima yang terlibat dalam fosforilasi oksidatif. Bertanggung jawab untuk mengambil keuntungan dari energi gradien elektrokimia untuk membentuk ATP.
Protein transmembraal ini terdiri dari dua komponen: f0 dan f1. Komponen f0 memungkinkan pengembalian proton ke matriks mitokondria berfungsi sebagai saluran dan f1 mengkatalisasi sintesis ATP melalui ADP dan Pyo, Menggunakan energi pengembalian tersebut.
Dapat melayani Anda: protein konveyor membran: fungsi dan jenisProses sintesis ATP membutuhkan perubahan struktural dalam f1 dan perakitan komponen f0 dan f1. Translokasi proton melalui f0 Itu menyebabkan perubahan konformasi dalam tiga subunitas f1, memungkinkan ini bertindak sebagai mesin rotasi, mengarahkan pembentukan ATP.
Subunit yang bertanggung jawab atas penyatuan ADP dengan pyo berubah dari keadaan lemah (l) ke aktif (t). Saat ATP terbentuk, subunit kedua beralih ke keadaan terbuka (O) yang memungkinkan pelepasan molekul ini. Setelah ATP dirilis, subunit ini beralih dari keadaan terbuka ke keadaan tidak aktif (L).
Molekul ADP dan Pyo Mereka bergabung dengan subunit yang telah berubah dari negara bagian atau negara bagian l.
Produk
Rantai dan fosforilasi konveyor elektron menghasilkan molekul ATP. Oksidasi NADH menghasilkan sekitar 52,12 kkal/mol (218 kJ/mol) dari energi bebas.
Reaksi global untuk oksidasi NADH adalah:
Nadh+1⁄2 atau2 +H+ ↔ h2O+nad+
Transfer elektron dari Nadh dan fadh2 Ini terjadi melalui beberapa kompleks, memungkinkan perubahan energi bebas ΔG ° dibagi menjadi "paket" yang lebih kecil, yang digabungkan dengan sintesis ATP.
Oksidasi molekul NADH menghasilkan sintesis tiga molekul ATP. Sedangkan oksidasi molekul fadh2 Itu melekat pada sintesis dua ATP.
Koenzim ini berasal dari proses glikolisis dan siklus asam sitrat. Untuk setiap molekul glukosa terdegradasi, molekul ATP 36 atau 38 berakhir, tergantung pada lokasi sel. Di otak dan otot rangka 36 ATP diproduksi sementara 38 ATP diproduksi dalam jaringan otot.
Fungsi
Semua organisme, uniseluler dan multiseluler, membutuhkan energi minimum dalam sel mereka untuk melakukan proses di dalamnya, dan pada gilirannya mempertahankan fungsi vital dalam tubuh yang lengkap.
Proses metabolisme membutuhkan energi untuk dilakukan. Sebagian besar energi yang dapat digunakan diperoleh dengan degradasi karbohidrat dan lemak. Energi ini berasal dari proses fosforilasi oksidatif.
Kontrol fosforilasi oksidatif
Laju penggunaan ATP dalam sel, mengontrol sintesis yang sama, dan pada gilirannya, karena kopling fosforilasi oksidatif dengan rantai transpor elektron, juga umumnya mengatur laju transportasi elektronik.
Fosforilasi oksidatif memiliki kontrol ketat yang memastikan bahwa ATP tidak dihasilkan lebih cepat dari yang dikonsumsi. Ada langkah -langkah tertentu dalam proses transportasi elektron dan fosforilasi digabungkan yang mengatur laju produksi energi.
Kontrol terkoordinasi produksi ATP
Rute produksi energi utama (ATP sel) adalah glikolisis, siklus asam sitrat dan fosforilasi oksidatif. Kontrol terkoordinasi dari ketiga proses ini mengatur sintesis ATP.
Kontrol fosforilasi dengan rasio aksi massa ATP tergantung pada kontribusi yang tepat dari elektron dalam rantai conveyoring. Ini pada gilirannya tergantung pada hubungan [nadh]/[nad+] yang dipertahankan ditinggikan oleh aksi glikolisis dan siklus asam sitrat.
Kontrol terkoordinasi ini dilakukan dengan mengatur titik kontrol glikolisis (sitrat menghambat PFK) dan siklus asam sirat (dehidrogenase piruvat, cutease sitrat, dehidrogenase gort-chitrate dan dehidrogenase α-zetoglutarate))).
Kontrol oleh akseptor
Kompleks IV (sitokrom C oksidase) adalah enzim yang diatur oleh salah satu substratnya, yaitu aktivitasnya dikendalikan oleh pengurangan sitokrom C (c2+), yang pada gilirannya seimbang dengan hubungan konsentrasi antara [nadh]/[nad+] dan rasio aksi massa [ATP]/[ADP] + [pyo].
Itu dapat melayani Anda: nada: karakteristik dan fungsiSemakin tinggi [NADH]/[NAD+] dan turunkan [ATP]/[ADP]+[pyo], lebih banyak konsentrasi akan menjadi sitokrom [c2+] dan lebih besar akan menjadi aktivitas IV kompleks. Ini ditafsirkan, misalnya, jika kita membandingkan organisme dengan aktivitas istirahat yang berbeda dan aktivitas tinggi.
Pada individu dengan aktivitas fisik yang tinggi, konsumsi ATP dan oleh karena itu hidrolisisnya ke ADP + Pyo Ini akan sangat tinggi, menghasilkan perbedaan dalam rasio aksi massa yang menyebabkan peningkatan [c2+dan oleh karena itu peningkatan sintesis ATP. Pada individu yang beristirahat, situasi sebaliknya terjadi.
Pada akhirnya, kecepatan fosforilasi oksidatif meningkat dengan konsentrasi ADP dalam mitokondria. Konsentrasi ini tergantung pada penerjemah ADP-ATP yang bertanggung jawab atas pengangkutan nukleotida adenin dan pyo Dari sitosol ke matriks mitokondria.
Agen dekakoplan
Fosforilasi oksidatif dipengaruhi oleh agen kimia tertentu, yang memungkinkan transportasi elektronik berlanjut tanpa fosforilasi ADP, memisahkan produksi dan konservasi energi.
Agen -agen ini merangsang kecepatan konsumsi oksigen mitokondria tanpa adanya ADP, juga menyebabkan peningkatan hidrolisis ATP. Mereka bertindak dengan menghilangkan perantara atau memecahkan keadaan energi dari rantai konveyor elektron.
2,4-dinitrofenol, asam lemah yang melewati membran mitokondria, bertanggung jawab untuk menghilangkan gradien proton, karena mereka bergabung dengan mereka di sisi asam dan melepaskannya di sisi dasar.
Senyawa ini digunakan sebagai "pil pelangsing" karena ditemukan bahwa ia menghasilkan peningkatan pernapasan, oleh karena itu, peningkatan laju metabolisme dan penurunan berat badan terkait. Namun, ditunjukkan bahwa efek negatifnya bahkan dapat menyebabkan kematian.
Disipasi gradien protonik menghasilkan panas. Sel jaringan adiposa coklat menggunakan decoupling, terkontrol secara hormon, untuk menghasilkan panas. Mamalia hibernasi dan bayi baru lahir yang kekurangan rambut terdiri dari jaringan ini yang berfungsi sebagai semacam selimut termal.
Inhibitor
Senyawa atau agen penghambat mencegah konsumsi atau2 (transportasi elektronik) seperti fosforilasi oksidatif terkait. Agen -agen ini menghindari pembentukan ATP melalui penggunaan energi yang diproduksi dalam transportasi elektronik. Oleh karena itu, rantai transportasi berhenti karena konsumsi energi seperti itu tidak diatur.
Antibiotik oligomisin bekerja sebagai penghambat fosforilasi pada banyak bakteri, mencegah stimulasi ADP dari sintesis ATP.
Ada juga agen ionofor, yang membentuk kompleks yang larut dengan lemak dengan kation seperti k+ dan na+, dan melewati membran mitokondria dengan kation ini. Mitokondria kemudian menggunakan energi yang diproduksi dalam transportasi elektronik untuk memompa kation alih -alih mensintesis ATP.
Referensi
- Alberts, b., Bray, d., Hopkin, k., Johnson, a., Lewis, J., Raff, m., Roberts, k. & Walter, P. (2004). Biologi Sel Esensial. New York: Ilmu Garland.
- Cooper, g. M., Hausman, r. DAN. & Wright, n. (2010). Sel. (hal. 397-402). Marbán.
- Devlin, t. M. (1992). Buku Teks Biokimia: Dengan Korelasi Klinis. John Wiley & Sons, Inc.
- Garrett, r. H., & Grisham, C. M. (2008). Biokimia. Thomson Brooks/Cole.
- Lodish, h., Darnell, J. DAN., Berk, a., Kaiser, c. KE., Krieger, m., Scott, m. P., & Matsudaira, P. (2008). Biologi Sel Molekular. Macmillan.
- Nelson, d. L., & Cox, m. M. (2006). Prinsip -prinsip biokimia lehninger Edisi ke -4. Ed Omega. Barcelona.
- Voet, d., & Voet, J. G. (2006). Biokimia. Ed. Pan -American Medical.
- « Karakteristik Euglenophyta, Reproduksi, Nutrisi, Klasifikasi
- Pelatihan, fungsi, dan jenis/kelompok glukosida »

