Gaya kohesi
- 4967
- 842
- Tommie Smith
Apa itu kekuatan kohesi?
Itu kekuatan kohesi Mereka adalah gaya tarik antarmolekul yang menjaga beberapa molekul dengan yang lain. Bergantung pada intensitas gaya kohesi, suatu zat dalam keadaan padat, cair atau gas. Nilai gaya kohesi adalah sifat intrinsik dari setiap zat.
Properti ini terkait dengan bentuk dan struktur molekul masing -masing zat. Karakteristik penting dari kekuatan kohesi adalah bahwa mereka berkurang dengan cepat ketika jarak meningkat. Kemudian, mereka disebut gaya kohesi ke gaya tarik yang terjadi antara molekul zat yang sama.
Itu Kekuatan penolakan Mereka adalah mereka yang dihasilkan dari energi kinetik (energi karena pergerakan) partikel. Energi ini menyebabkan molekul terus bergerak. Intensitas gerakan ini berbanding lurus dengan suhu di mana zat tersebut.
Untuk menyebabkan perubahan status suatu zat, perlu menaikkan suhunya dengan transmisi panas. Ini menyebabkan kekuatan tolakan zat meningkat, yang, jika berlaku, dapat berakhir dengan asumsi perubahan keadaan.
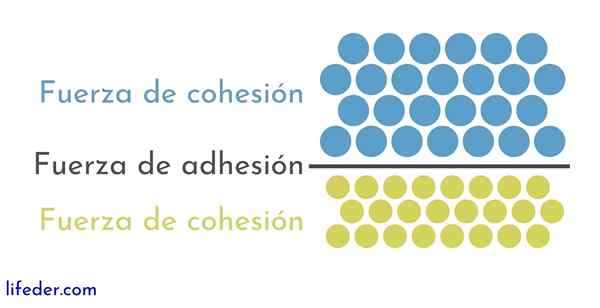
Di sisi lain, penting dan perlu untuk membedakan antara kohesi dan adhesi:
- Kohesi disebabkan oleh gaya tarik antara partikel yang berdekatan dari zat yang sama.
- Adhesi adalah hasil interaksi yang terjadi antara permukaan zat atau tubuh yang berbeda.
Kedua kekuatan ini tampak terkait dengan beberapa fenomena fisik yang mempengaruhi cairan, jadi penting pemahaman yang baik dari satu dan yang lainnya.
Ini dapat melayani Anda: Vy Canis Majoris: Penemuan, Karakteristik, Struktur, Pelatihan dan EvolusiGaya kohesi dalam padatan, cairan dan gas
 Atom dalam tiga keadaan utama materi
Atom dalam tiga keadaan utama materi Dalam padatan
Secara umum, dalam kekuatan kohesi padatan sangat tinggi dan diberikan secara intens di tiga arah ruang.
Dengan cara ini, jika gaya eksternal diterapkan pada tubuh padat, perpindahan kecil molekul terjadi satu sama lain.
Selain itu, ketika gaya eksternal menghilang, gaya kohesi cukup kuat untuk kembali ke molekul dalam posisi semula, memulihkan posisi sebelum penerapan gaya.
Dalam cairan
Sebaliknya, dalam cairan, gaya kohesi hanya tinggi di dua arah spasial, sementara mereka sangat lemah di antara lapisan cairan.
Dengan demikian, ketika suatu gaya diterapkan dalam arah tangensial pada cairan, gaya ini memecah ikatan yang lemah di antara lapisan. Ini menyebabkan lapisan cair menyelinap di atas yang lain.
Kemudian, ketika penerapan gaya berakhir, gaya kohesi tidak memiliki kekuatan yang cukup untuk menempatkan kembali molekul cair dalam posisi aslinya.
Selain itu, dalam cairan, kohesi juga tercermin dalam tegangan permukaan, yang disebabkan oleh gaya tidak seimbang yang diarahkan ke bagian dalam cairan, yang bekerja pada molekul permukaan.
Demikian juga, kohesi juga diamati ketika transisi dari keadaan cair ke keadaan padat diberikan, karena efek kompresi molekul cair.
Dalam gas
Dalam gas, kekuatan kohesi tercela. Dengan cara ini, molekul Gase berada dalam gerakan konstan, karena dalam kasus mereka gaya kohesi tidak dapat menjaga mereka tetap saling terkait.
Dapat melayani Anda: Keuntungan Mekanik: Formula, Persamaan, Perhitungan, dan ContohOleh karena itu, dalam gas, gaya kohesi dapat dilihat hanya ketika proses pencairan terjadi, yang terjadi ketika molekul gas dikompresi dan kekuatan tarik cukup kuat untuk menghasilkan transisi gas keadaan ke keadaan cair keadaan cair.
Contoh kekuatan kohesi
Seringkali kekuatan kohesi dikombinasikan dengan kekuatan adhesi untuk menimbulkan fenomena fisik dan kimia tertentu.
Sebagai contoh, kekuatan kohesi bersama -sama dengan adhesi memungkinkan untuk menjelaskan beberapa fenomena paling umum yang terjadi pada cairan; Ini adalah kasus meniskus, ketegangan permukaan dan kapilaritas.
Oleh karena itu, dalam kasus cairan perlu untuk membedakan antara gaya kohesi, yang terjadi antara molekul cairan yang sama; dan adhesi, yang terjadi antara molekul cairan dan padatan.
Tegangan permukaan

Tegangan permukaan adalah gaya yang terjadi secara tangensial dan per satuan panjang di tepi permukaan bebas cairan yang ada dalam kesetimbangan. Kekuatan ini mengontrak permukaan cairan.
Pada akhirnya, tegangan permukaan terjadi karena gaya yang terjadi dalam molekul cair berbeda pada permukaan cairan daripada yang terjadi di dalam.
Meniskus
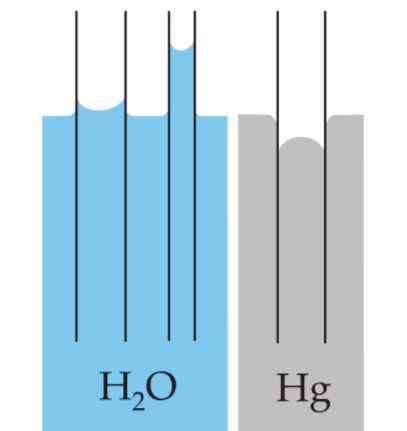
Kelengkungan yang dibuat di permukaan cairan disebut meniskus saat dikurung dalam wadah. Kurva ini dihasilkan oleh efek yang dimiliki permukaan wadah pada cairan yang mengandungnya.
Dapat melayani Anda: Meter TekananKurva dapat menjadi cembung atau cekung, tergantung pada apakah gaya antara molekul cairan dan yang dari wadah adalah daya tarik - seperti halnya air dan kaca - atau penolakan, seperti halnya antara merkuri dan kaca.
Kapilaritas
 Contoh kapilaritas
Contoh kapilaritas Kapilaritas adalah sifat cairan yang memungkinkan mereka naik atau turun melalui tabung kapiler. Itu adalah properti yang memungkinkan, sebagian, munculnya air di dalam tanaman.
Cairan naik melalui tabung kapiler saat gaya kohesi lebih rendah daripada adhesi antara cairan dan dinding tabung. Dengan cara ini, cairan akan terus naik sampai nilai tegangan permukaan sama dengan berat cairan yang terkandung dalam tabung kapiler.
Sebaliknya, jika gaya kohesi lebih tinggi daripada adhesi, tegangan permukaan akan turun ke cairan dan bentuk permukaannya akan menjadi cembung.
Referensi
- Kohesi (kimia) (n.D.). Di Wikipedia. Diterima dari.Wikipedia.org.
- Tegangan permukaan (n.D.). Di Wikipedia. Diterima dari.Wikipedia.org.
- Kapilaritas (n.D.). Di Wikipedia. Pulih dari es.Wikipedia.org.
- Iran. Levine; "Fisikokimia" Volume 1; Edisi Kelima; 2004; MC Graw Hillm.
- Moore, John W.; Stanitski, Conrad L.; Jurs, Peter C. (2005). Kimia: Ilmu Molekuler. Belmont, CA: Brooks/Cole.
- Putih, Harvey dan. (1948). Fisika Perguruan Tinggi Modern. Van Nostrand.


