Fondasi, teknik, dan penggunaan uji katalase

- 2767
- 639
- Joseph Nader PhD
Itu katalase Ini adalah metodologi yang digunakan dalam laboratorium bakteriologi untuk menyoroti keberadaan enzim katalase pada bakteri yang memilikinya. Di sebelah pewarnaan Gram adalah tes utama yang harus dilakukan pada mikroorganisme yang baru diisolasi. Tes ini memandu ahli mikrobiologi pada langkah -langkah yang harus diikuti untuk identifikasi definitif mikroorganisme yang dimaksud.
Secara umum, bakteri yang mengandung sitokrom memiliki enzim catlase, yaitu, bakteri anaerob aerobik dan opsional harus memilikinya. Namun, ada pengecualian, seperti Streptococcus, yang meskipun mikroorganisme anaerob opsional tidak memiliki enzim katalase.
 Eksekusi uji katalase, menunjukkan reaksi positif. Sumber: Tidak ada penulis yang dapat dibaca mesin yang disediakan. Nase diasumsikan (berdasarkan klaim hak cipta). [CC BY-SA 3.0 (http: // createveCommons.Org/lisensi/by-sa/3.0/]]
Eksekusi uji katalase, menunjukkan reaksi positif. Sumber: Tidak ada penulis yang dapat dibaca mesin yang disediakan. Nase diasumsikan (berdasarkan klaim hak cipta). [CC BY-SA 3.0 (http: // createveCommons.Org/lisensi/by-sa/3.0/]] Itulah sebabnya uji katalase terutama digunakan untuk membedakan Staphylococaee dan Micrococaceae (keduanya katalase positif) dari keluarga Streptococaee (negatif katalase) (negatif katalase).
Demikian juga, genus Bacillus (katalase positif) dibedakan dari genus Clostridium (negatif katalase), antara lain.
[TOC]
Dasar
Catalase adalah enzim yang diklasifikasikan sebagai hidroperoksidase, ini berarti mereka menggunakan hidrogen peroksida sebagai substrat (h2SALAH SATU2).
Ini juga dianggap sebagai oksidoreduktase, karena dalam reaksi di mana ada elemen yang berfungsi sebagai donor elektron (zat pereduksi) dan lainnya sebagai penerima elektron (zat pengoksidasi).
Catalase adalah protein yang mengandung kelompok prostorik dengan empat atom besi trivalen (Faith+++), oleh karena itu homoprotein. Ion besi tetap teroksidasi selama reaksi.
Dapat dikatakan bahwa katalase adalah enzim detoksifikasi, karena fungsinya adalah untuk menghilangkan zat yang terjadi selama metabolisme bakteri yang beracun bagi bakteri. Di antara zat -zat ini adalah hidrogen peroksida.
Hidrogen peroksida terbentuk dari dekomposisi gula oleh aerobik. Proses ini terjadi sebagai berikut:
Ion superoksida (atau2-) (Radikal bebas) dibentuk sebagai produk akhir dari asimilasi glukosa dengan jalan aerobik. Ini beracun dan dieliminasi oleh enzim superoksida dismutase yang mengubahnya menjadi oksigen gas dan hidrogen peroksida.
Itu dapat melayani Anda: Holdridge Life Zone: Apa yang ada di Amerika LatinHidrogen peroksida juga beracun bagi bakteri dan harus dihilangkan. Enzim katalase membuka hidrogen peroksida dalam air dan oksigen.
Katalase dapat bertindak pada substrat lain selain hidrogen peroksida, seperti alkohol, aldehida, asam, amina aromatik dan fenol. Namun, hidrogen peroksida juga dapat digunakan dengan katalase untuk mengoksidasi senyawa toksik lainnya seperti metil dan etil alkohol.
Demikian juga, katalase hadir dalam sel fagositik, melindunginya dari aksi toksik hidrogen peroksida.
Teknik rutin untuk uji katalase
-Metode dalam slide
Bahan
3% hidrogen peroksida (10 volume).
Lamina portabel
Pegangan plastik sekali pakai atau tongkat kayu.
Prosedur
Mengambil jumlah yang cukup dari koloni untuk belajar tanpa menyentuh agar dari mana asalnya. Koloni harus segar, yaitu, dari tanaman 18 hingga 24 jam.
Tempatkan koloni pada dudukan kering dan di atasnya tambahkan setetes hidrogen peroksida 3% (Anda juga dapat menggunakan h2SALAH SATU2 di 30%). Amati segera jika gelembung dilepas atau tidak.
Penafsiran
Reaksi positif: Detasemen gas, yang terbukti dengan pembentukan gelembung (gelembung yang kuat).
Reaksi Negatif: Tidak ada pembentukan gelembung.
-Metode langsung dalam budaya murni
Tempatkan 1 ml h2SALAH SATU2 3% pada tanaman murni dalam piring atau irisan yang tidak mengandung darah (lebih disukai pegangan bergizi). Perhatikan apakah ada pembentukan gelembung atau tidak. Anda juga dapat menggunakan h2SALAH SATU2 30%.
Itu ditafsirkan seperti metode pemegang objek.
-Metode dengan tabung kapiler atau fung dan petrishko
Isi tabung kapiler 67 mm pada ketinggian 20 mm dengan 3% hidrogen peroksida per kapilaritas.
Sentuh koloni terisolasi yang ingin Anda pelajari dengan kapiler penuh h2SALAH SATU2 3%. Amati jika kapiler diisi dengan gelembung dalam waktu sekitar 10 detik. Metode ini memungkinkan untuk semi-kuantifikasi reaksi di persilangan:
Tanpa persilangan tidak ada gelembung (reaksi negatif).
Dapat melayani Anda: Flora dan Fauna Kepulauan Falkland: Spesies Luar Biasa+ --Gelembung yang langka (reaksi lemah atau tertunda).
++ -Gelembung berlimpah (reaksi sedang).
+++ -Gelembung mencapai ujung yang berlawanan (reaksi energik).
-Metode Taylor dan Achanzar untuk tes katalase yang memberikan keraguan
Dalam slide yang bersih dan kering meletakkan koloni yang terisolasi, lalu letakkan setetes h2SALAH SATU2 0,5% dan tutupi dengan sampul. Perhatikan apakah ada pembentukan gelembung yang dipenjara atau tidak.
Interpretasi: Kehadiran gelembung menunjukkan reaksi positif. Tanpa gelembung, itu ditafsirkan sebagai reaksi negatif.
Uji katalase untuk spesies Mycobacterium
Teknik ini perlu dilakukan dengan mengendalikan pH dan suhu. Itu harus dieksekusi di bawah lonceng aliran laminar, karena manipulasi spesies mycobacterium yang berbeda berbahaya.
-Bahan
30% atau 110 volume hidrogen peroksida (superoxal).
Buffer fosfat pH 7
Tween 80 hingga 10%
Kultur mycobacterium dalam wedge dari 3 hingga 4 minggu
-Persiapan dari reagen
Buffer fosfat pH 7
Menimbang:
1.361 g (KH2PO4) Anhydra.
1.420 g (Na2HPO3) Dysodic Phosphate Anhydrous.
Larutkan kedua garam dalam sedikit air suling steril dan lengkap dengan air hingga 1000 mL.
Tween 80 hingga 10%
Lakukan pengenceran 1:10 untuk Tween 80 yang datang secara komersial, untuk ini melanjutkan sebagai berikut:
Ambil 1 ml Tween 80 dan letakkan di dalam sedikit air suling, larut dan kemudian lengkapi volume dengan air hingga 10 mL.
Reagen akhir
Campur sejumlah buffer fosfat dengan jumlah tween 80 hingga 10% (di bagian yang sama). Tentukan di laboratorium seberapa banyak Anda ingin mempersiapkan.
-Prosedur
Tempatkan 5 mL buffer fosfat dalam tabung reaksi steril dengan tutup ulir (Baquelita).
Dengan pegangan inokulasi, ambil koloni yang cukup dari pertumbuhan mycobacterium yang ditaburkan dalam irisan dan larut dalam buffer fosfat.
Tutupi tabung tanpa mengencangkan benang. Tempatkan di kamar mandi pada suhu 68 ° C selama 20 hingga 30 menit. Keluarkan dan dinginkan pada 22-25 ° C
Ukur 0,5 mL reagen akhir (campuran) dan tambahkan ke tabung dengan larutan dingin. Mengamati atau tidak Formasi Bubble.
Itu ditafsirkan serta teknik sebelumnya.
Menggunakan
Ketika pertumbuhan koloni di media yang diperkaya diperoleh, pewarnaan gram dan tes katalase harus dilakukan ke koloni yang diperoleh. Ini akan memandu ahli mikrobiologi tentang prosedur yang harus diikuti untuk identifikasi definitif.
Dapat melayani Anda: epitel datar sederhana: karakteristik, fungsi dan jenis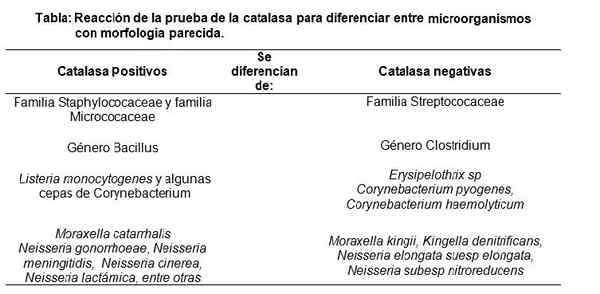 Sumber: Disiapkan oleh Penulis MSC. Marielsa Gil
Sumber: Disiapkan oleh Penulis MSC. Marielsa Gil Qa
Untuk mengevaluasi fungsi yang tepat dari reagen hidrogen peroksida, gunakan kontrol yang baru dibudidayakan, seperti Staphylococcus aureus sebagai kontrol dan ketegangan positif Streptococcus sp sebagai kontrol negatif.
Alternatif lain yang berfungsi sebagai kontrol positif adalah menempatkan setetes hidrogen peroksida pada agar darah, eritrosit memiliki katalase, oleh karena itu, akan ada gelembung jika reagen dalam kondisi baik.
Anda dapat menggunakan agar cokelat sebagai kontrol negatif, di sini eritrosit sudah terdaftar dan tes memberikan negatif.
Batasan
-Jangan gunakan tanaman lama untuk pengujian, karena ini dapat menyebabkan negatif palsu.
-Hindari mengambil koloni dari tanaman dalam agar darah, jika Anda berhati -hati untuk tidak menyentuh agar; Prosedur ini dapat menyebabkan positif palsu, karena eritrosit mengandung katalase.
-Jika Anda mengambil koloni dengan pegangan platinum, jangan menginvestasikan urutan prosedur karena ini dapat menghasilkan positif palsu. Ini karena platinum mampu bereaksi dengan hidrogen peroksida, berasal dari gelembung.
-Jangan gunakan reagen hidrogen peroksida jika sudah sangat tua, karena reagennya sangat tidak stabil dan cenderung rusak seiring waktu.
-Jaga agar reagen hidrogen peroksida terlindungi dari cahaya dan pendingin untuk mencegah kerusakan.
-Melakukan kontrol kualitas untuk reagen hidrogen peroksida setiap kali digunakan.
-Memperhitungkan bahwa jika h digunakan2SALAH SATU2 Pada 30% reaksi lebih kuat dari yang dilakukan dengan H2SALAH SATU2 3%.
Referensi
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Diagnosis mikrobiologis. Edisi ke -5. Pan -American Editorial S.KE. Argentina.
- Forbes B, Sahm D, Weissfeld A. (2009). Diagnosis mikrobiologis Bailey & Scott. 12 ed. Pan -American Editorial S.KE. Argentina.
- Mac Faddin J. (2003). Tes biokimia untuk identifikasi bakteri pentingnya klinis. Edisi ke -3. Editorial Pan -American. Buenos Aires. Argentina.
- Laboratorium BD. Reagen katalase. Tersedia di: http: // winklerltda.Cl
- Laboratorium Vadequímica. Hidrogen peroksida. Kesetaraan antara volume dan persentase. Tersedia di: Vadequimica.com

