Struktur Tembaga Sulfat (CUSO4), Properti, Perolehan, Penggunaan
- 4662
- 1386
- Dewey Runolfsdottir
Dia tembaga sulfat Ini adalah senyawa anorganik yang dibentuk oleh elemen tembaga (Cu), sulfur (S) dan oksigen (O) (O). Formula kimianya adalah cuso4. Tembaga berada dalam keadaan oksidasi +2, sulfur +6, dan oksigen memiliki valencia -2.
Itu adalah padatan putih bahwa ketika terpapar kelembaban lingkungan menjadi pentahidrat biru cuso -nya4 •5H2SALAH SATU. Padatan putih diperoleh dengan memanaskan biru untuk menghilangkan air.
 Tembaga sulfat (cuo4) anhidrat (tanpa air dalam struktur kristalnya). W. Oelen/CC BY-SA (https: // createveCommons.Org/lisensi/by-sa/3.0). Sumber: Wikimedia Commons.
Tembaga sulfat (cuo4) anhidrat (tanpa air dalam struktur kristalnya). W. Oelen/CC BY-SA (https: // createveCommons.Org/lisensi/by-sa/3.0). Sumber: Wikimedia Commons. Ini telah digunakan sebagai agen antibakteri selama berabad -abad untuk menyembuhkan luka pada manusia dan hewan. Ini juga berfungsi sebagai fungisida, sebagai astringen, antidiare dan mengendalikan penyakit usus pada hewan. Ini juga digunakan sebagai agen antihongos pada tanaman.
Namun, beberapa kegunaannya telah dihentikan karena kelebihannya dapat beracun bagi manusia, hewan dan tumbuhan. Interval konsentrasi di mana ia dapat digunakan adalah sempit dan tergantung pada spesies.
Ini digunakan sebagai katalis dalam reaksi kimia dan sebagai pelarut kering. Ini memungkinkan untuk meningkatkan resistensi dan fleksibilitas beberapa polimer.
Jumlah berlebih dari senyawa ini dapat berbahaya bagi tanah, karena beracun bagi mikroorganisme yang bermanfaat bagi tanaman.
[TOC]
Struktur
Tembaga sulfat dibentuk oleh ion tembaga (Cu2+) dan ion sulfat (jadi42-).
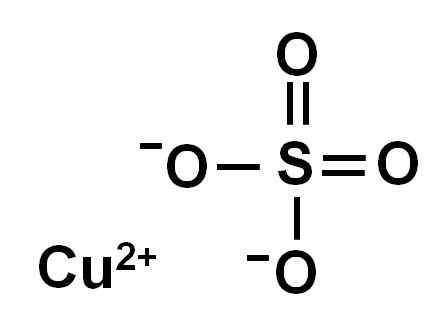 Ionica Copper Sulfate (II). Penulis: Marilú Stea.
Ionica Copper Sulfate (II). Penulis: Marilú Stea. Karena hilangnya dua elektron, ion tembaga (II) memiliki konformasi elektronik berikut:
1s2 2s2 2 p6 3S2 3p6 3d9
Dapat dilihat bahwa orbital memiliki 3d tidak lengkap (memiliki 9 elektron, bukan 10).
Tata nama
- Anhidrat tembaga sulfat
- Tembaga sulfat (II)
- Cupric sulfat
Properti
Keadaan fisik
Padatan putih kehijauan atau kristal -berbentuk.
Berat molekul
159.61 g/mol
Titik lebur
Pada 560 ºC itu rusak.
Kepadatan
3,60 g/cm3
Kelarutan
22 g/100 g air pada 25 ° C. Tidak larut dalam etanol.
Sifat kimia
Saat itu mengalami kelembaban udara di bawah 30 ° C, itu menjadi senyawa pentahidrat cuso4 •5H2SALAH SATU.
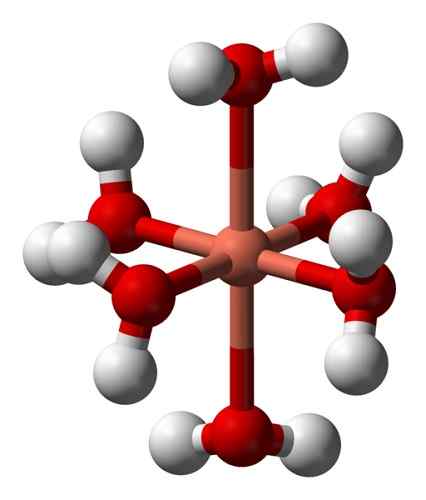
Solusi berairnya berwarna biru karena pembentukan ion hexaacuocobre (II) [Cu (H2SALAH SATU)6]2+ yang menghasilkan warna seperti itu. Dalam ion ini dua molekul air lebih jauh dari atom logam dari empat lainnya.
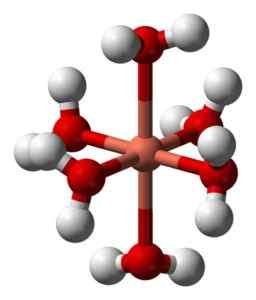 Struktur Ion Hexaacuocobre (II) [Cu (H (H (H2SALAH SATU)6]2+. Benjah-bmm27 / domain publik. Sumber: Wikimedia Commons.
Struktur Ion Hexaacuocobre (II) [Cu (H (H (H2SALAH SATU)6]2+. Benjah-bmm27 / domain publik. Sumber: Wikimedia Commons. Ini karena apa yang disebut efek Jahn-Teller, yang memprediksi bahwa jenis sistem ini mengalami distorsi yang disebabkan oleh fakta bahwa Cu2+ Ini memiliki struktur elektronik yang berakhir dengan D9, yaitu orbital yang tidak lengkap (akan lengkap jika itu d10).
Dapat melayani Anda: kalsium hidroksida (ca (oh) 2): struktur, sifat, mendapatkan, menggunakanJika amonia ditambahkan (NH3) Solusi ini terbentuk di mana NH3 Molekul air secara berturut -turut menggusur. Mereka dibentuk misalnya dari [Cu (NH3) (H2SALAH SATU)5]2+ Sampai [Cu (NH3)4(H2SALAH SATU)2]2+.
Saat cuso4 Itu dipanaskan hingga dekomposisinya memancarkan gas beracun dan menjadi oksida cupric.
Memperoleh
Anhidrat tembaga sulfat dapat diperoleh dengan dehidrasi total senyawa pentahidrat, yang dicapai dengan memanaskannya sampai molekul air menguap.
Cuso4 •5H2O + panas → cuo4 + 5 jam2Atau ↑
Senyawa pentahidrat berwarna biru, sehingga air cuso diperoleh saat kehilangan air kristalisasi4 Anhidrat putih.
Aplikasi
Beberapa penggunaannya tumpang tindih dengan senyawa pentahidrat. Lainnya khusus untuk zat anhidrat.
Sebagai agen antibakteri
Ini memiliki potensi sebagai agen antimikroba. Ini telah digunakan selama ribuan tahun, bahkan dalam budaya Amerika Selatan dan Amerika Tengah, untuk mencegah infeksi luka melalui kain kasa yang diresapi dalam larutan senyawa ini.
Diperkirakan bahwa dalam mekanisme aktivitas antibakteri ion Cu2+ Mereka membentuk chelate dengan enzim yang sangat penting untuk fungsi seluler bakteri, menonaktifkannya. Mereka juga menginduksi pembentukan radikal hidroksil OH •, yang merusak membran bakteri dan DNA mereka.
 Cuso4 Itu dapat bekerja melawan beberapa bakteri patogenik. Penulis: Gerd Altmann. Sumber: Pixabay.
Cuso4 Itu dapat bekerja melawan beberapa bakteri patogenik. Penulis: Gerd Altmann. Sumber: Pixabay. Baru -baru ini telah dilaporkan bahwa cuso jejak4 Mereka dapat meningkatkan aktivitas antimikroba dari produk alami yang kaya polifenol, seperti ekstrak granat dan infus dari beberapa jenis tanaman teh.
Dalam aplikasi hewan
Ini digunakan sebagai antiseptik dan astringen untuk membran lendir dan untuk mengobati konjungtivitis eksternal dan otitis. Ini berfungsi untuk melakukan mandi terapeutik atau profilaksis untuk menghindari pembusukan sapi, domba, dan mamalia lainnya.
 Solusi Cuo Aqueous4 Mereka berfungsi untuk menyembuhkan lubang ternak. Penulis: Ingrid und Stefan Melichar. Sumber: Pixabay.
Solusi Cuo Aqueous4 Mereka berfungsi untuk menyembuhkan lubang ternak. Penulis: Ingrid und Stefan Melichar. Sumber: Pixabay. Ini berfungsi sebagai agen kaustik untuk massa nekrotik di ekstremitas sapi, borok stomatitis dan jaringan granulasi ini. Ini telah digunakan sebagai fungisida dalam pengobatan pewarna dan penyakit yang disebabkan oleh jamur kulit.
Ini juga digunakan sebagai emético (agen untuk memancing muntah) pada babi, anjing dan kucing; sebagai antidiareal astringen untuk anak sapi dan mengendalikan moniliasis usus dalam trikomoniasis unggas dan kalkun.
Sebagai suplemen pakan ternak
Tembaga sulfat telah digunakan sebagai suplemen dalam jumlah yang sangat kecil untuk memberi makan sapi, babi dan unggas. Itu berfungsi untuk mengobati kekurangan tembaga dalam ruminansia. Dalam kasus babi dan burung itu digunakan sebagai stimulan pertumbuhan.
Dapat melayani Anda: kromatogramTembaga telah diidentifikasi sebagai penting untuk biosintesis hemoglobin pada mamalia, struktur kardiovaskular, sintesis kolagen tulang, sistem enzim dan reproduksi.
Seperti disebutkan di bagian sebelumnya, ini juga dapat disuplai sebagai obat untuk pengendalian penyakit. Namun, suplementasi dan/atau tingkat obat harus dipantau dengan hati -hati.
 Burung kandang dan telurnya dapat dipengaruhi oleh kelebihan tembaga sulfat dalam diet mereka. Penulis: Pexels. Sumber: Pixabay.
Burung kandang dan telurnya dapat dipengaruhi oleh kelebihan tembaga sulfat dalam diet mereka. Penulis: Pexels. Sumber: Pixabay. Dari jumlah tertentu, yang tergantung pada masing -masing spesies, dapat penurunan pertumbuhan, kehilangan nafsu makan dan berat, kerusakan pada organ tertentu dan bahkan kematian hewan dapat terjadi.
Misalnya, pada ayam suplementasi 0,2% atau lebih mengurangi konsumsi makanan ini dengan konsekuensi penurunan berat badan, penurunan produksi telur dan ketebalan kulitnya.
Dalam aplikasi pertanian
Dalam sistem produksi organik tidak diperbolehkan menggunakan fungisida sintetis, hanya produk tembaga dan sulfur yang diterima, seperti tembaga sulfat.
Misalnya, jamur tertentu yang menyerang tanaman apel, seperti Venturia inaequealis, dihilangkan dengan senyawa ini. Diperkirakan bahwa mungkin ion cu2+ Mereka dapat memasuki spora jamur, mendenaturalisasi protein dan memblokir beberapa enzim.
 Tembaga sulfat berfungsi untuk memerangi beberapa jamur yang menyerang apel. Algirdas di LT.Wikipedia / domain publik. Sumber: Wikimedia Commons.
Tembaga sulfat berfungsi untuk memerangi beberapa jamur yang menyerang apel. Algirdas di LT.Wikipedia / domain publik. Sumber: Wikimedia Commons. Pentingnya tembaga pada tanaman
Elemen tembaga penting dalam proses fisiologis tanaman seperti fotosintesis, pernapasan dan pertahanan terhadap antioksidan. Baik kekurangan elemen ini dan kelebihannya menghasilkan spesies teroksigenasi reaktif yang berbahaya bagi molekul dan strukturnya.
Interval konsentrasi tembaga untuk pertumbuhan dan pengembangan tanaman yang optimal sangat sempit.
Efek samping pada pertanian
Ketika produk ini terlalu banyak digunakan dalam kegiatan pertanian, itu bisa fitotoksik, menyebabkan pengembangan buah -buahan dini dan mengubah warnanya.
Selain itu, tembaga menumpuk di tanah dan beracun bagi mikroorganisme dan cacing tanah. Ini bertentangan dengan konsep pertanian organik.
 Meskipun cuso4 Ini digunakan dalam pertanian organik dapat berbahaya bagi cacing bumi. Penulis: Patricia Maine Degrave. Sumber: Pixabay.
Meskipun cuso4 Ini digunakan dalam pertanian organik dapat berbahaya bagi cacing bumi. Penulis: Patricia Maine Degrave. Sumber: Pixabay. Tentang reaksi kimia
Cuso4 Anhidrat berfungsi sebagai katalis untuk beberapa reaksi senyawa organik karbonil dengan diol atau epoksida, membentuk diokolan atau asetonid. Berkat senyawa ini reaksi dapat dilakukan dalam kondisi lunak.
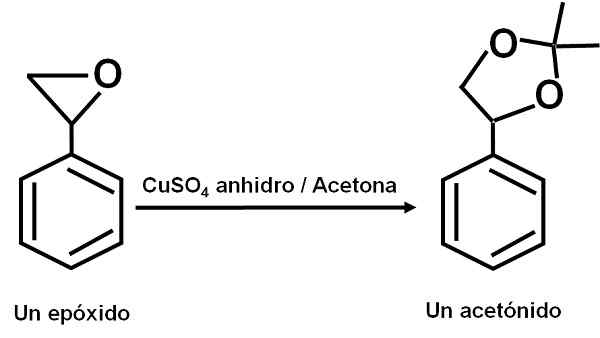 Contoh reaksi di mana cuso4 anhydrous bertindak sebagai katalisator. Penulis: Marilú Stea.
Contoh reaksi di mana cuso4 anhydrous bertindak sebagai katalisator. Penulis: Marilú Stea. Juga telah dilaporkan bahwa aksi katalitiknya memungkinkan untuk mendehidrasi alkohol sekunder, tersier, benzil dan alilik ke olefin yang sesuai. Reaksi dilakukan dengan cara yang sangat sederhana.
Dapat melayani Anda: anetolAlkohol murni dipanaskan bersama dengan cuso4 Anhidrat pada suhu 100-160 ° C untuk waktu 0,5-1,5 jam. Dengan demikian, dehidrasi alkohol dan olefin terjadi, distil murni dari campuran reaksi.
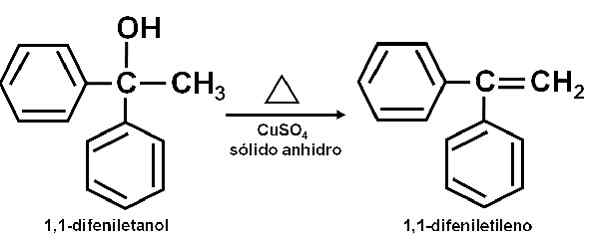 Dehidrasi alkohol untuk tembaga sulfat (ii) anhidrat. Penulis: Marilú Stea.
Dehidrasi alkohol untuk tembaga sulfat (ii) anhidrat. Penulis: Marilú Stea. Sebagai agen dehidrasi
Senyawa ini digunakan di laboratorium kimia sebagai pengeringan. Itu berfungsi untuk mendehidrasi cairan organik seperti pelarut. Menyerap air yang membentuk senyawa pentahidrat cuo4 •5H2SALAH SATU.
 Saat cuso4 Anhydro putih menyerap air menjadi senyawa pentahidrat biru4.5H2SALAH SATU. Crystal Titan/CC BY-SA (https: // CreativeCommons.Org/lisensi/by-sa/4.0). Sumber: Wikimedia Commons.
Saat cuso4 Anhydro putih menyerap air menjadi senyawa pentahidrat biru4.5H2SALAH SATU. Crystal Titan/CC BY-SA (https: // CreativeCommons.Org/lisensi/by-sa/4.0). Sumber: Wikimedia Commons. Untuk meningkatkan polimer
Cuso4 Anhydro telah digunakan untuk meningkatkan sifat -sifat polimer tertentu dan pada saat yang sama memungkinkan mereka untuk didaur ulang.
Sebagai contoh, partikel senyawa aseton telah dicampur dengan karet acrylonitrile-butadiene dalam pabrik khusus, mencoba membuat partikel cuso4 Menjadi sangat kecil.
Tembaga sulfat meningkatkan titik serikat polimer yang membentuk campuran dengan resistensi tinggi, kekerasan dan fleksibilitas yang mengejutkan.
Dalam aplikasi terapi yang dihentikan
Di masa lalu, larutan tembaga sulfat untuk pencucian lambung digunakan ketika seseorang menderita keracunan fosfor putih. Namun, solusinya segera diaduk untuk menghindari keracunan tembaga.
Larutan senyawa ini juga digunakan bersama dengan zat lain untuk luka bakar topikal di kulit dengan fosfor.
Terkadang mereka melayani dalam bentuk nutrisi tertentu.
Lotion tertentu untuk eksim, impetigo dan intertrigo berisi cuo4. Solusi digunakan sebagai astringen dalam infeksi mata. Terkadang kristal diaplikasikan langsung pada luka bakar atau bisul.
Semua aplikasi ini tidak lagi dibuat karena toksisitas yang dapat menyebabkan senyawa berlebih.
Referensi
- ATAU.S. Perpustakaan Kedokteran Nasional. (2019). Tembaga sulfat. Pulih dari pubchem.NCBI.Nlm.Nih.Pemerintah.
- Timah, d.R. (Editor) (2003). Buku Pegangan Kimia dan Fisika CRC. 85th CRC Press.
- Montag, J. et al. (2006). Studi in vitro tentang Venturia inaequealis. J. Agric. Makanan makanan. 2006, 54, 893-899. Tautan pulih.Peloncat.com.
- Holloway, a.C. et al. (2011). Peningkatan aktivitas antimikroba dari teh putih utuh dan sub-fraksi dengan kecanduan tembaga (II) sulfat dan vitamin C terhadap Staphylococcus aureus; Untuk pendekatan mekanistik. BMC Complement Alternal Med 11, 115 (2011). Diperoleh dari BMCCLomplementMedtherapies.Biomedcentral.com.
- Sanz, a. et al. (2018). Mekanisme penyerapan tembaga Arabidopsis Thalia Transporter High -Finity Copt. Protoplasma 256, 161-170 (2019). Tautan pulih.Peloncat.com.
- Griminger, hlm. (1977). Efek tembaga sulfat pada produksi telur dan ketebalan cangkang. Ilmu Unggas 56: 359-351, 1977. Pulih dari akademik.Oup.com.
- Hanzlik, r.P. Dan Leinwetter, m. (1978). Reaksi senyawa epoksida dan karbonil yang dikatalisis oleh tembaga sulfat anhidrat. J. Org. Chem., Vol.43, no.3, 1978. Pulih dari pub.ACS.org.
- Okonkwo, a.C. et al. (1979). Persyaratan tembaga babi babi diberi makan diet murni. Jurnal Nutrisi, Volume 109, Edisi 6, Juni 1979, Halaman 939-948. Pulih dari akademik.Oup.com.
- Hoffman, r.V. et al. (1979). Tembaga Anhidrat (II) Sulfat: Efisien. J. Org. Chem., 1980, 45, 917-919. Pulih dari pub.ACS.org.
- Shao, c. et al. (2018). Kekuatan tarik yang ditingkatkan dari komposit karet akrilonitril-butadien/komposit tembaga anhidrat yang disiapkan dengan koordinasi silang-linking. Polim. Banteng. 76, 1435-1452 (2019). Tautan pulih.Peloncat.com.
- Betts, J.W. et al. (2018). Antibakteri baru: alternatif antibiotik tradisional. Tembaga. Dalam kemajuan fisiologi mikroba. Pulih dari scientedirect.com
- Kapas, f. Albert dan Wilkinson, Geoffrey. (1980). Kimia anorganik canggih. Edisi keempat. John Wiley & Sons.
- Situs Google. Buat sulfat tembaga anhidrat. Dalam kimia rumah paradoks. Pulih dari situs.Google.com.

