Struktur seng oksida (ZnO), sifat, penggunaan, risiko
- 1141
- 315
- Domingo Gutkowski
Dia Seng oksida Ini adalah senyawa anorganik yang formula kimianya adalah Zno. Itu hanya terdiri dari ion Zn2+ SAYA2- dalam rasio 1: 1; Namun, jaringan kristalnya dapat menghadirkan lowongan atau2-, yang memberi tempat cacat struktural yang mampu mengubah warna kristal sintetisnya.
Secara komersial diperoleh sebagai padatan putih berdebu (gambar bawah), yang terjadi langsung dari oksidasi seng logam oleh proses Prancis; atau mengalami pengurangan karbotermik pada bijih seng, sehingga uapnya kemudian mengoksidasi dan mengakhiri pemadatan.
 Kaca jam dengan seng oksida. Sumber: Adam Rędzikowski [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)]
Kaca jam dengan seng oksida. Sumber: Adam Rędzikowski [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)] Metode persiapan ZnO lainnya terdiri dari memicu hidroksida mereka, Zn (OH)2, Dari larutan air garam seng. Juga, film bagus atau nanopartikel yang bervariasi secara morfologis dapat disintesis dengan teknik yang lebih canggih seperti deposisi kimia uapnya.
Oksida logam ini ditemukan di alam sebagai mineral zinit, yang kristal biasanya kuning atau oranye karena kotoran logam. Kristal ZnO ditandai dengan menjadi piezoelektrik, termokromatik, luminescent, polar, dan juga memiliki pita energi yang sangat luas dalam sifat semikonduktornya.
Secara struktural, isomorfik ke seng sulfida, Zns, mengadopsi kristal heksagonal dan kubik yang mirip dengan wurzita dan blenda, masing -masing. Dalam hal ini ada karakter kovalen tertentu dalam interaksi antara Zn2+ SAYA2-, yang membuat distribusi beban yang heterogen dalam kristal ZnO.
Studi tentang sifat dan penggunaan ZnO meluas ke bidang fisika, elektronik dan biomedis. Penggunaannya yang paling sederhana dan paling sehari -hari tidak diperhatikan dalam komposisi krim wajah dan produk kebersihan pribadi, serta di tabir surya.
[TOC]
Struktur
Polimorf
Zno mengkristal dalam kondisi tekanan dan suhu normal dalam struktur heksagonal wurzite. Dalam struktur ini ion Zn2+ SAYA2- Mereka diatur dalam lapisan alternatif, sehingga masing -masing berakhir dikelilingi oleh tetrahedron, memiliki Zno4 atau ozn4, masing -masing.
Juga, menggunakan "templat" atau dukungan kubik, ZnO dapat dikristalisasi dalam struktur kubik blenda seng; Yang, seperti Wurzita, sesuai dengan struktur isomorfik (identik dalam ruang tetapi dengan ion yang berbeda) dari seng sulfida, Zns.
Selain dua struktur ini (Wurzita dan Blenda), ZnO di bawah tekanan tinggi (sekitar 10 GPa) mengkristal dalam struktur Sal Gema, sama dengan NaCl.
Dapat melayani Anda: Referensi Elektroda: Karakteristik, Fungsi, ContohInteraksi
Interaksi antara Zn2+ SAYA2- Mereka menyajikan karakter kovalensi tertentu, jadi ada sebagian ikatan kovalen Zn-O (keduanya atom dengan hibridisasi SP3), dan karena distorsi tetrahedra, mereka memanifestasikan momen dipol yang menambah atraksi ionik dari kristal Zno.
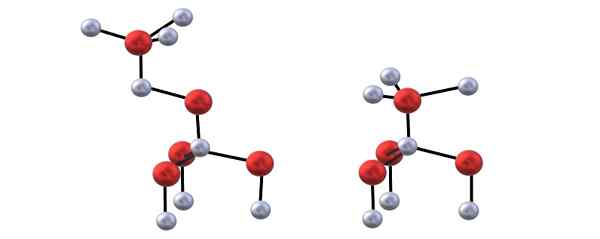
 Struktur Blenda (kiri) dan Wurzita (kanan) ZnO. Sumber: Gabriel Bolívar.
Struktur Blenda (kiri) dan Wurzita (kanan) ZnO. Sumber: Gabriel Bolívar. Anda memiliki gambar atas untuk memvisualisasikan tetrahedra yang disebutkan di atas untuk struktur ZnO.
Perbedaan antara blenda dan struktur wurzita juga terletak pada apa yang dapat Anda lihat dari atas, ion tidak ditemukan dikalahkan. Misalnya, di Wurzita, dapat dilihat bahwa bola putih (Zn2+) tepat di atas bola merah (atau2-). Di sisi lain, dalam struktur kubik blenda itu tidak terjadi karena ada tiga lapisan: a, b dan c bukan hanya dua.
Morfologi Nanopartikel
Kristal Zno Meskipun mereka cenderung memiliki struktur heksagonal wurzite, sehubungan dengan morfologi nanopartikel mereka adalah cerita lain. Bergantung pada parameter dan metode sintesis, ini dapat mengadopsi bentuk bervariasi seperti batang, pelat, daun, bola, bunga, ikat pinggang, jarum, antara lain.
Properti
Penampilan fisik
Putih solid, toilet dan rasanya pahit padat. Di alam dapat dikristalisasi, dengan kotoran logam, sebagai mineral zincita. Jika kristal seperti itu putih, mereka memiliki termokromisme, yang berarti bahwa ketika mereka mengubah warna: dari putih menjadi kuning.
Demikian juga, kristal sintetis mereka dapat menghadirkan warna kemerahan atau kehijauan tergantung pada komposisi oksigen stoikiometrik mereka; yaitu, lubang atau lowongan yang disebabkan oleh kurangnya anion atau2- secara langsung mempengaruhi cara cara berinteraksi dengan jaringan ion.
Masa molar
81.406 g/mol
Titik lebur
1974 ºC. Pada suhu ini, dekomposisi termal menderita dengan melepaskan seng dan oksigen molekuler atau oksigen gas.
Kepadatan
5.1 g/cm3
Kelarutan air
ZnO praktis tidak larut dalam air, nyaris tidak menimbulkan solusi dengan konsentrasi 0,0004% hingga 18 ° C.
Anfoterisme
ZnO dapat bereaksi baik dengan asam dan basa. Saat bereaksi dengan asam dalam larutan berair, kelarutannya meningkat ketika garam yang larut terbentuk di mana Zn2+ akhirnya mengomplekskan dengan molekul air: [Zn (oh2)6]2+. Misalnya, bereaksi dengan asam sulfat untuk menghasilkan seng sulfat:
ZnO + H2Sw4 → Znso4 + H2SALAH SATU
Demikian pula bereaksi dengan asam lemak untuk membentuk garam masing -masing, seperti stearat dan seng palmitat.
Dapat melayani Anda: reaksi ireversibel: karakteristik dan contohDan ketika bereaksi dengan alas, di hadapan air, garam chisal terbentuk:
Zno + 2naoh + h2O → na2[Zn (OH)4]
Kapasitas panas
40.3 j/k · mol
Kesenjangan energi langsung
3.3 EV. Nilai ini dibuat oleh semikonduktor broadband, mampu beroperasi di bawah medan listrik yang intens. Ini juga menyajikan karakteristik menjadi semikonduktor tipe N, yang belum dapat menjelaskan alasan bahwa ada kontribusi ekstra elektron dalam strukturnya.
Oksida ini dibedakan dengan sifat optik, akustik dan elektroniknya, berkat yang dianggap sebagai kandidat untuk aplikasi potensial yang terkait dengan pengembangan perangkat optoelektronik (sensor, laser, sel fotovoltaik). Alasan properti seperti itu lolos dari bidang fisika.
Aplikasi
Obat
Lima oksida telah digunakan sebagai aditif dalam banyak krim putih untuk pengobatan iritasi, jerawat, dermatitis, lecet dan retakan pada kulit. Di daerah ini, penggunaannya untuk meringankan iritasi yang disebabkan oleh popok pada kulit bayi sangat populer.
Ini juga merupakan komponen tabir surya, karena bersama dengan nanopartikel titanium dioksida2, Membantu memblokir radiasi ultraviolet matahari. Demikian juga, itu bertindak sebagai agen yang lebih tebal, jadi itu adalah makeup, lotion, enamel, talcos, dan sabun tertentu yang jelas.
Di sisi lain, ZnO adalah sumber lima belas yang digunakan dalam suplemen makanan dan produk vitamin, serta dalam sereal.
Antibakteri
Menurut morfologi nanopartikelnya, ZnO dapat diaktifkan di bawah radiasi ultraviolet untuk menghasilkan hidrogen peroksida atau spesies reaktif yang melemahkan membran sel mikroorganisme.
Ketika ini terjadi, nanopartikel yang tersisa dari ZnO melintasi sitoplasma dan mulai berinteraksi dengan ringkasan biomolekul yang membentuk sel, yang dihasilkan sebagai konsekuensi apoptosisnya.
Itulah sebabnya tidak semua nanopartikel dapat digunakan dalam komposisi tabir surya, tetapi hanya mereka yang tidak memiliki aktivitas antibakteri.
Produk dengan jenis ZnO ini dialokasikan, ditutupi dengan bahan polimer terlarut, untuk mengobati infeksi, luka, bisul, bakteri dan bahkan diabetes.
Pigmen dan pelapis
Pigmen yang dikenal sebagai Cinco Blanco adalah ZnO, yang ditambahkan ke beberapa lukisan dan pelapis untuk melindungi permukaan logam dari korosi di mana mereka diterapkan. Misalnya, pelapis ZnO yang kecanduan digunakan untuk melindungi besi galvanis.
Di sisi lain, pelapis ini juga telah digunakan pada gelas jendela untuk mencegah panas menembus (jika di luar negeri) atau masuk (jika di dalam). Ini juga melindungi beberapa bahan polimer dan tekstil dari kemundurannya dengan aksi radiasi matahari dan panas.
Dapat melayani Anda: kalium (k)Bioimaging
Luminesensi nanopartikel ZnO telah dipelajari untuk digunakan dalam bioimaging, sehingga belajar melalui lampu biru, hijau atau oranye yang memancar, struktur internal sel.
Aditif
ZnO juga menemukan penggunaan sebagai aditif dalam karet, semen, bahan dentifric, kaca dan keramik, karena titik lelehnya yang lebih rendah dan, oleh karena itu, berperilaku seperti agen pendiri.
Eliminator hidrogen sulfida
ZnO menghilangkan gas h yang tidak menyenangkan2S, membantu desulfur beberapa emanasi gase:
ZnO + H2S → ZnS + H2SALAH SATU
Risiko
Finch oksida seperti itu adalah senyawa yang tidak beracun dan tidak berbahaya, sehingga manipulasi yang bijaksana dari padatannya tidak mewakili risiko apa pun.
Namun masalahnya terletak pada asapnya, karena meskipun pada suhu tinggi membusuk, uap Rav akhirnya mencemari paru -paru dan menyebabkan semacam "demam logam". Penyakit ini ditandai dengan gejala batuk, demam, perasaan penindasan di dada, dan rasa logam yang konstan di mulut.
Cancerigen juga tidak, dan krim yang mengandungnya belum menunjukkan bahwa mereka meningkatkan penyerapan seng pada kulit, sehingga matahari berbasis ZnO dianggap aman; Kecuali ada reaksi alergi, yang dalam hal ini harus menghentikan penggunaannya.
Mengenai nanopartikel tertentu yang ditujukan untuk memerangi bakteri, ini dapat memberikan efek negatif jika tidak diangkut dengan benar ke tempat tindakan mereka.
Referensi
- Shiver & Atkins. (2008). Kimia anorganik. (Edisi keempat). MC Graw Hill.
- Wikipedia. (2019). Seng oksida. Diperoleh dari: di.Wikipedia.org
- Hadis Morkoç dan ümit Özgur. (2009). Seng oksida: teknologi fundamental, bahan dan perangkat. [PDF]. Dipulihkan dari: Aplikasi.Wiley-VCH.dari
- Parihar, m. Raja dan r. Paulose. (2018). Tinjauan singkat tentang sifat struktural, listrik dan elektrokimia nanopartikel seng oksida. [PDF]. Dipulihkan dari: IPME.Ru
- KE. Rodnyi dan saya. V. Khodyuk. (2011). Sifat optik dan luminesensi seng oksida. Pulih dari: arxiv.org
- Siddiqi, k. S., Ur Rahman, untuk., Tajuddin, & husen, a. (2018). Sifat nanapartikel seng oksida dan aktivitas ES terhadap mikroba. Surat Penelitian Nanoscale, 13 (1), 141. Doi: 10.1186/S11671-018-2532-3
- ChemicalSafetyFacts. (2019). Seng oksida. Pulih dari: chemicalsafetyfacts.org
- Jinhuan Jiang, Jiang Pi, dan Jiye Cai. (2018). Kemajuan nanopartikel seng oksida untuk aplikasi biomedis. Kimia dan Aplikasi Bioinorganik, Vol. 2018, artikel ID 1062562, 18 halaman. doi.org/10.1155/2018/1062562
- « Struktur hidrogen peroksida (H2O2), sifat, penggunaan, mendapatkan
- Struktur natrium sulfat (Na2SO4), sifat, penggunaan, mendapatkan »

