Struktur Sodium Cyanide (NACN), Properti, Risiko, Penggunaan

- 2674
- 552
- Pete Lesch
Dia Sodium sianida Ini adalah garam anorganik yang dibentuk oleh na kation natrium+ dan cn anion sianida-. Formula kimianya adalah Nacn. Juga dikenal sebagai natrium sianida, itu adalah padatan kristal putih. Ini higroskopis, yaitu, menyerap air dari lingkungan, dan kristal -kristalnya adalah kubik seperti natrium klorida NaCl.
Saat larut dalam air, ia cenderung membentuk hcn hidrogen sianida. Solusinya larut emas dan perak dengan mudah. Fitur ini membuatnya digunakan untuk mengekstrak emas dan perak dari mineral -minerya. Solusi yang digunakan untuk tujuan ini didaur ulang, yaitu, mereka digunakan kembali beberapa kali.
 Natrium natrium sianida. L26 [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)]. Sumber: Wikimedia Commons.
Natrium natrium sianida. L26 [CC BY-SA 4.0 (https: // createveCommons.Org/lisensi/by-sa/4.0)]. Sumber: Wikimedia Commons. Namun, beberapa sianida berhasil melarikan diri dari kolam limbah tertentu, yang mewakili bahaya bagi fauna dan manusia, karena sianida sangat beracun dan dapat menyebabkan kematian.
NACN digunakan dalam industri kimia sebagai perantara untuk menyiapkan beberapa jenis senyawa, seperti pewarna, bahan kimia untuk pertanian dan obat -obatan atau obat -obatan.
Sodium sianida adalah senyawa yang sangat berbahaya karena dapat menyebabkan kematian, jadi harus dimanipulasi dengan sangat hati -hati.
[TOC]
Struktur
Sodium sianida dibentuk oleh ion Na+ dan ion CN-.
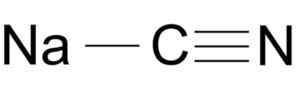 Nacn Struktur Molekul Sodium Cyanide. Arrowsmaster [domain publik], Sumber: Wikimedia Commons.
Nacn Struktur Molekul Sodium Cyanide. Arrowsmaster [domain publik], Sumber: Wikimedia Commons. Ion sianida memiliki mobil mobil dan salah satu nitrogen dan bersatu satu sama lain oleh triple link.
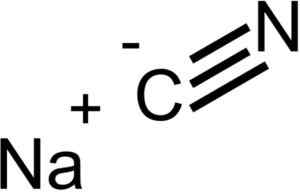 Ion yang membentuk natrium sianida nacn. EPOP [domain publik]. Sumber: Wikimedia Commons.
Ion yang membentuk natrium sianida nacn. EPOP [domain publik]. Sumber: Wikimedia Commons. NACN memiliki struktur kristal yang sama dengan NaCl, jadi kristalnya adalah kubik.
Tata nama
-Sodium sianida
-Sodium sianida
Properti
Keadaan fisik
Padatan kristal putih higroskopis (menyerap air dari lingkungan).
Berat molekul
49.007 g/mol
Titik lebur
563.7 ºC
Titik didih
1496 ºC
Titik nyala
Itu tidak mudah terbakar. Tetapi jika terpapar api, hcn hidrogen sianida dan nitrogen oksida terjadi.
Dapat melayani Anda: Sublimasi: Konsep, Proses, dan ContohKepadatan
1.595 g/cm3 pada 20 ºC
Kelarutan
Sangat larut dalam air: 48 g/100 ml pada 10ºC, 82 g/100 ml pada suhu 35 ° C. Sedikit larut dalam alkohol
Konstan disosiasi
Itu dihidrolisis dalam larutan berair yang menghasilkan hidrogen sianida HCN. Konstanta hidrolisis ini adalah kH = 2,5 x 10-5.
ph
Larutan berair NACN sangat basa
Sifat kimia
Saat larut dalam air, ia terpisah dalam ion -ionnya+ dan cn-. Dalam larutan berair, ion sianida CN- Ambil proton h+ air h2Atau membentuk hcn dan ion oh-, Jadi solusinya menjadi basa.
Cn- + H2O → hcn + oh-
Untuk alasan ini, larutan air mereka terurai dengan cepat dengan tetap disimpan, membentuk HCN hidrogen sianida.
Itu korosif menuju aluminium. Solusinya dengan mudah melarutkan AU dan AG perak di hadapan udara.
Ini adalah agen pengkelat karena anion sianida CN- Ini dapat dengan mudah bergabung dengan logam lain, seperti perak, emas, merkuri, seng, kadmium, dll.
Menyajikan aroma lemah almond pahit.
Risiko
Harus ditangani dengan sangat hati -hati. Ini adalah senyawa yang sangat beracun, menghambat proses metabolisme yang penting, dan menyebabkan kematian baik untuk konsumsi, inhalasi, penyerapan kulit atau kontak mata.
Jika NACN dihirup, ia larut dalam mukosa saluran pernapasan dan diteruskan ke aliran darah. Ion sianida NACN memiliki afinitas yang kuat terhadap zat besi dalam keadaan oksidasi +3, yaitu, iman kation besi3+.
Saat sianida diserap, ia bereaksi dengan cepat dengan iman3+ enzim penting mitokondria sel (sitokrom oksidase), mencegah proses pernapasan tertentu dilakukan.
Oleh karena itu, respirasi seluler dihambat atau pengereman dan hipoksia sitotoksik. Itu berarti bahwa sel dan jaringan tidak dapat menggunakan oksigen, terutama sel otak dan jantung.
Dengan cara ini, kerusakan permanen atau mematikan pada tubuh terjadi. Ini bisa terjadi baik pada manusia maupun hewan.
Jika kemacetan pembuluh darah dan korosi mukosa lambung sedang menelan, di samping apa yang telah disebutkan.
Dapat melayani Anda: Justus von Liebig Sodium cyanide nacn dapat menyebabkan kematian. Penulis: Openicons. Sumber: Pixabay.
Sodium cyanide nacn dapat menyebabkan kematian. Penulis: Openicons. Sumber: Pixabay. Itu bukan bahan bakar, tetapi bersentuhan dengan asam, melepaskan hcn yang sangat mudah terbakar dan beracun.
Jika meleleh dengan nitrit atau klorat, itu dapat mengeksploitasi.
Memperoleh
Itu dapat diperoleh dengan natrium na, amonia NH3 dan batubara c. Sodium bereaksi dengan amonia yang memberikan natrium nanh2:
2 Na + 2 NH3 → 2 Nanh2 + H2↑
Sodium amida dipanaskan dengan karbon pada 600 ºC dan menghasilkan natrium cyanamide NA2NCN, yang kemudian dengan batubara pada 800 ° C menjadi natrium sianida:
2 Nanh2 + C → 2 H2↑ + na2NCN
Na2NCN + C → 2 NACN
Metode lain adalah melelehkan kalsium dan sianamida batubara C dengan natrium karbonat NA2BERSAMA3:
Cancn + c + na2BERSAMA3 → Caco3 + 2 Nacn
Itu juga dapat disiapkan dengan melewati gas nitrogen n2 untuk campuran panas natrium karbonat2BERSAMA3 dan bubuk batubara C, menggunakan iman iman sebagai katalis atau akselerator reaksi:
Na2BERSAMA3 + 4 c + n2 → 2 NACN + 3 CO ↑
Aplikasi
Dalam ekstraksi mineral emas dan perak. Konsekuensi
Sodium sianida telah digunakan sejak lama untuk mengekstrak logam emas dan perak dari mineral.
Sianida yang digunakan dalam proses ini didaur ulang, tetapi sesuatu keluar dari kolam limbah bersama dengan logam berat yang tidak pulih.
Burung, kelelawar, dan hewan lain yang minum dari laguna ini dengan sianida telah diracuni.
Ada catatan bendungan Rumania yang membuat kolam limbah terisolasi dan rusak oleh peristiwa cuaca.
Sebagai akibatnya, berton -ton sianida dilepaskan ke Sungai Sasar dan sistem akuifer di dekatnya seperti Laus, Somes, Tisza Rivers, yang berakhir di Danube.
Ini menyebabkan air terjun kematian hewan, atau dengan kata lain, bencana ekologis.
 Ekstraksi emas dengan sianida di Selandia Baru sekitar tahun 1918. Anda dapat melihat jumlah air yang terkontaminasi, yang dikeluarkan di sungai terdekat. Perpustakaan Nasional NZ on the Commons [tidak ada batasan]. Sumber: Wikimedia Commons.
Ekstraksi emas dengan sianida di Selandia Baru sekitar tahun 1918. Anda dapat melihat jumlah air yang terkontaminasi, yang dikeluarkan di sungai terdekat. Perpustakaan Nasional NZ on the Commons [tidak ada batasan]. Sumber: Wikimedia Commons. Dalam produksi senyawa kimia lainnya
Sodium sianida NACN digunakan dalam sintesis berbagai jenis senyawa organik.
Dapat melayani Anda: natrium oksida (na2o): struktur, rumus, sifat, risikoMisalnya, pigmen dan pewarna disiapkan (termasuk polesan optik), senyawa untuk digunakan dalam pertanian atau agrokimia dan berbagai produk farmasi.
Ini juga berfungsi untuk mendapatkan agen chelating atau penculikan ion logam.
Dengan natrium sianida, senyawa yang disebut nitril disiapkan, yang bila diobati dengan asam asam atau larutan berair alkali memungkinkan untuk mendapatkan asam karboksilat.
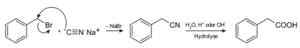 Persiapan asam karboksilat menggunakan natrium sianida NACN. Roland Mattern [domain publik]. Sumber: Wikimedia Commons.
Persiapan asam karboksilat menggunakan natrium sianida NACN. Roland Mattern [domain publik]. Sumber: Wikimedia Commons. Ini memungkinkan untuk menyiapkan asam lemak dengan gugus siano, sianida logam berat dan hidrogen sianida HCN.
Di industri logam
NACN digunakan dalam solusi yang digunakan dalam galvanoplasty atau elektroda logam (lapisan logam dengan yang lain) misalnya seng.
Ini adalah komponen baja yang dikeraskan. Itu juga berfungsi dalam pembersihan logam.
Dalam kegunaan lain
Sodium sianida adalah perantara dalam pembuatan nilon.
Ini digunakan untuk memisahkan mineral dengan pengapungan dengan busa.
Aplikasi tidak digunakan, ditanya atau sangat jarang
Bangsa ini digunakan untuk menghilangkan hewan pengerat, seperti kelinci dan tikus dan liang mereka, dan untuk mengakhiri sarang rayap.
Saat ini digunakan sesekali untuk menghilangkan coyote, rubah dan anjing liar. Ini digunakan dalam bentuk kapsul sebagai dosis sederhana atau berganda di tanah penggembalaan, perburuan dan hutan.
Karena toksisitas ekstremnya, NACN hanya harus digunakan oleh orang yang siap.
Penggunaan ini dianggap sangat berbahaya bagi manusia, tetapi ada yang masih menggunakannya.
 Kehidupan liar tidak boleh dihilangkan, karena hewan -hewan ini sudah berjuang untuk bertahan hidup dalam kondisi sulit. Penulis: Maxwdhs. Sumber: Pixabay.
Kehidupan liar tidak boleh dihilangkan, karena hewan -hewan ini sudah berjuang untuk bertahan hidup dalam kondisi sulit. Penulis: Maxwdhs. Sumber: Pixabay. Di pertanian itu sebelumnya digunakan untuk fumigasi pohon buah jeruk dan buah -buahan lainnya. Itu juga digunakan sebagai insektisida dan mitida (tungau eliminator) untuk diaplikasikan setelah panen, untuk jeruk yang tidak disimpan atau untuk pengasingan truk yang digunakan untuk mengangkutnya. Itu juga digunakan untuk fumigasi kapal, kereta api dan gudang.
Semua kegunaan ini telah dipertanyakan oleh toksisitas tinggi natrium sianida. Untuk alasan ini, ini tidak lagi digunakan atau hanya sangat jarang dan dalam kondisi yang sangat terkontrol.
Referensi
- ATAU.S. Perpustakaan Kedokteran Nasional. (2019). Sodium sianida. Pulih dari pubchem.NCBI.Nlm.Nih.Pemerintah.
- Kirk-Othmer (1994). Encyclopedia of Chemical Technology. Edisi keempat. John Wiley & Sons.
- Hurst, h.DAN. dan Martin, m.D. (2017). Toksikologi. Sianida. Dalam Farmakologi dan Terapi untuk Kedokteran Gigi (Edisi Ketujuh). Pulih dari scientedirect.com.
- Coppock, r.W. dan dziwenka, m. (2015). Ancaman terhadap satwa liar oleh agen perang kimia. Dalam Buku Pegangan Toksikologi Agen Peperangan Kimia (Edisi Kedua). Pulih dari scientedirect.com.
- Morrison, r.T. dan Boyd, R.N. (2002). Kimia organik. Edisi ke -6. Prentice-Hall.
- « Struktur Sulfur Trioksida (SO3), Properti, Risiko, Penggunaan
- Barium oksida (BAO) Struktur, sifat, penggunaan, risiko »

