Karakteristik sistein, struktur, fungsi, biosintesis
- 3075
- 403
- Ernesto Mueller
Itu Sistein (Cys, c) adalah salah satu dari 22 asam amino yang ditemukan di alam sebagai bagian dari rantai polipeptida yang membentuk protein makhluk hidup. Sangat penting untuk stabilitas struktur tersier protein, karena membantu pembentukan jembatan disulfida intramolekul.
Seperti halnya itu benar untuk asam amino lainnya seperti alanin, arginin, asparagin, glutamat dan glutamin, glisin, prolin, serin dan tirosin, manusia mampu mensintesis sistein, jadi ini tidak dianggap sebagai asam amino yang esensial amino yang esensi.
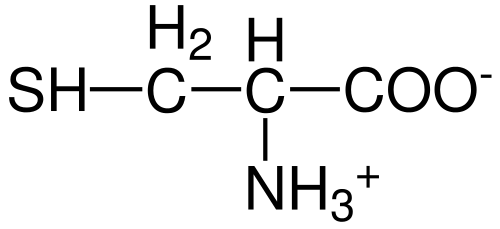
 Struktur Asam Amino Sistein (Sumber: Hattrich [Domain Publik] melalui Wikimedia Commons)
Struktur Asam Amino Sistein (Sumber: Hattrich [Domain Publik] melalui Wikimedia Commons) Terlepas dari ini, dan mengingat fakta bahwa laju sintesis tidak selalu memasok persyaratan tubuh, beberapa penulis menggambarkan sistein sebagai asam amino "kondisi" pada dasarnya ".
Asam amino ini dinamai oleh "Cystina", komponen perhitungan vesikular yang ditemukan pada tahun 1810, yang namanya diciptakan pada tahun 1832 oleh a. Baudrimont dan f. Malaguti. Beberapa tahun kemudian, pada tahun 1884, dan. Baumann menemukan bahwa sistein adalah produk dari reduksi sistin.
Setelah pekerjaan yang dilakukan oleh Bauman, pada tahun 1899, ditentukan bahwa sistein adalah konstituen utama protein yang membentuk tanduk berbagai hewan, yang menyarankan kemungkinan penggunaannya untuk sintesis polipeptida.
Saat ini diketahui bahwa sistein tubuh berasal dari makanan, daur ulang protein dan sintesis endogen, yang terjadi terutama pada hepatosit.
[TOC]
Karakteristik
Sistein memiliki berat molekul 121.16 g/mol dan ditemukan, bersama dengan leusin, isoleusin, valin, fenilalanin, triptofan, metionin dan tirosin, di antara asam amino hidrofobik yang paling hidrofobik.
Itu milik kelompok asam amino kutub tanpa beban dan, seperti asam amino lainnya, itu dapat terdegradasi oleh hidrolisis alkali pada suhu tinggi.
Seperti tryptophan, serin, glisin dan treonin, sistein adalah prekursor metabolik untuk glukoneogenesis dan ketogenesis (pembentukan tubuh keton).
Asam amino ini ada sebagai bagian dari urutan peptida protein, tetapi juga dapat bebas dalam plasma darah sebagai disulfida homogen (sistin, turunan) atau dicampur, terdiri dari bentuk homocysteine-sisteinine.
Perbedaan utama antara sistein bebas dan yang ditemukan dalam struktur protein adalah bahwa yang pertama dalam keadaan redoks yang sangat berkarat, sedangkan yang terakhir biasanya cukup berkurang.
Struktur
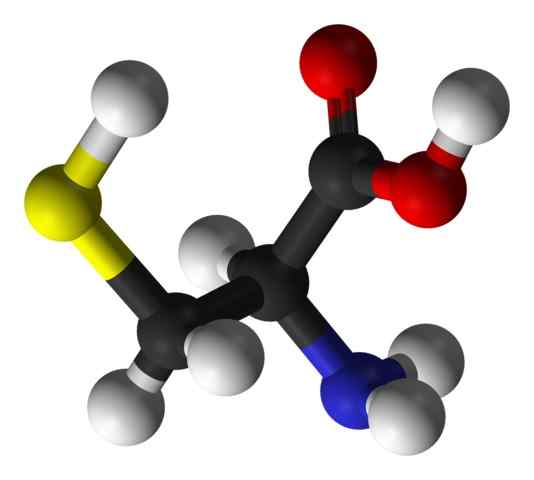
Seperti halnya asam amino lainnya yang dijelaskan hingga saat ini, sistein memiliki atom karbon sentral, yang bersifat kiral dan dikenal sebagai karbon α.
Empat spesies kimia yang berbeda bergabung dengan atom karbon ini:
- Grup amino (-NH3+)
- Grup karboksil (-co-)
- atom hidrogen dan
- Substituen (-r).
Kelompok substituen adalah yang memberikan identitas untuk setiap asam amino dan sistein ditandai dengan mengandung atom belerang sebagai bagian dari suatu kelompok Tiol salah satu Sulfhydrillo (-Ch2-sh).

Kelompok inilah yang memungkinkannya untuk berpartisipasi dalam pembentukan jembatan disulfida intra-intermolekul. Karena ini adalah nukleofil, Anda juga dapat berpartisipasi dalam reaksi substitusi.
Faktanya, rantai samping sistein ini dapat dimodifikasi untuk pembentukan dua senyawa yang dikenal sebagai "selenocysteine" dan "lantionine". Yang pertama adalah asam amino yang juga berpartisipasi dalam pembentukan protein dan yang kedua adalah turunan asam amino non -protein.
Dapat melayani Anda: histones: karakteristik, struktur, jenis dan fungsiKelompok Tiol Sistein juga ditandai dengan afinitasnya yang besar dengan ion perak dan merkuri (Ag+ dan Hg2+).
Fungsi
Fungsi utama sistein dalam organisme hidup berkaitan dengan partisipasi mereka dalam pembentukan protein. Secara khusus, sistein berpartisipasi dalam pembentukan jembatan disulfida, yang sangat penting untuk pembentukan struktur protein tersier.
Selain itu, asam amino ini tidak hanya berguna untuk sintesis protein, tetapi juga berpartisipasi dalam sintesis glutathione (GSH) dan memberikan pengurangan sulfur untuk metionin, asam lipoat, tiamin, koenzim A (COA), molybdopterine (kofaktor) dan lainnya Senyawa dengan kepentingan biologis.
Dalam kondisi jumlah berlebihan asam amino tersulfurisasi, sistein dan asam amino terkait lainnya dapat digunakan untuk produksi piruvat dan sulfur anorganik dan sulfur. Piruvat berhasil diarahkan ke rute glukoneogenik, melayani untuk produksi glukosa.
Keratin, yang merupakan salah satu jenis protein struktural yang paling banyak di kerajaan hewan, kaya akan residu sistein. Misalnya, wol domba mengandung lebih dari 4% belerang dari asam amino ini.
Sistein juga berpartisipasi dalam banyak reaksi reduksi oksida, jadi itu adalah bagian dari situs aktif beberapa enzim.
Saat bereaksi dengan glukosa, asam amino ini menghasilkan produk reaksi yang memperkenalkan selera dan aroma yang menarik pada beberapa persiapan kuliner.
Biosintesis
Biosintesis asam amino dalam tubuh manusia dan pada hewan lain (mamalia dan non-mamalia) terjadi dalam bentuk jaringan dan kelas sel; Ini adalah proses yang pantas mendapatkan energi dan biasanya dipisahkan antara organ yang berbeda.
Hati adalah salah satu organ utama yang terlibat dalam sintesis sebagian besar asam amino yang tidak penting, terlepas dari spesies yang dipertimbangkan.
Dalam hal ini tidak hanya sistein disintesis, tetapi juga aspartat, asparagin, glutamat dan glutamin, glisin, serin, tirosin dan lainnya dari prekursor asam amino spesifiknya.
Pada tahun 1935, merek Erwin menentukan bahwa sistein, pada mamalia, secara alami disintesis dari metionin, yang terjadi secara eksklusif di jaringan hati.
Proses ini dapat terjadi karena "transmetile" metionin, di mana gugus metil dipindahkan ke bukit dan creatine. Namun, sistein juga dapat dibentuk dari metionin berkat transulfurasi.
Selanjutnya ditunjukkan bahwa, selain metionin, beberapa senyawa sintetis seperti n-acetyl cysteine, cysteamine dan cystamin, adalah prekursor yang berguna untuk sintesis sistein sistein.
Dalam kasus sistein N-asetil, ini diambil oleh sel, di mana ia dikonversi menjadi sistein oleh enzim sitosol dalam sitosol.
Mekanisme sintesis
Mekanisme sintesis sistein dari metode yang paling terkenal adalah trans -ululo. Ini terjadi terutama di hati, tetapi juga telah ditentukan di usus dan pankreas.
Ini terjadi dari homocysteine, senyawa yang berasal dari metode asam amino; Dan reaksi pertama dari rute biosintetik ini adalah kondensasi yang dikatalisis oleh enzim cistationine β-sentase (CBS) (CBS).
Dapat melayani Anda: urasil: struktur, fungsi, sifat, sintesisEnzim ini mewakili bagian dari "komitmen" rute dan mengembun homocysteine dengan residu serin, asam amino protein lain, yang menghasilkan kistasiin. Selanjutnya, senyawa ini adalah "dipotong" atau "dibagi" oleh enzim Cistationasa, yang mengarah pada pelepasan sistein.
Regulasi aktivitas enzimatik CBS dimediasi oleh ketersediaan metode dan oleh keadaan redoks sel di mana proses ini terjadi.
Melalui rute sintesis sistein, sel dapat menangani metode berlebih, karena konversi mereka menjadi sistein adalah proses yang tidak dapat diubah.
Sintesis sistein pada tanaman dan mikroorganisme
Dalam organisme ini, sistein disintesis terutama dari sulfur anorganik, yang merupakan sumber sulfur yang paling banyak digunakan dalam biosfer aerobik.
Ini diambil, memasuki sel dan kemudian direduksi menjadi sulfida (S2-), yang dimasukkan ke dalam sistein dengan cara yang mirip dengan apa yang terjadi dengan amonium dalam sintesis glutamat atau glutamin.
Metabolisme dan degradasi
Katabolisme sistein terjadi terutama pada sel hati (hepatosit), meskipun juga dapat terjadi pada jenis sel lain seperti neuron, sel endotel dan sel otot polos pembuluh darah tubuh tubuh.
Cacat tertentu dalam katabolisme sistein menghasilkan penyakit herediter yang dikenal sebagai "sistinuria", ditandai dengan adanya perhitungan sistin di ginjal, kandung kemih dan ureter.
Sistin adalah asam amino yang berasal dari sistein dan perhitungan dibentuk oleh penyatuan dua molekul melalui atom belerangnya.
Bagian dari metabolisme sistein menghasilkan pembentukan asam ilmiah, dari mana adu banteng, asam amino non-proteik terbentuk. Reaksi dikatalisis oleh enzim dioxigenasa sistein.
Selain itu, sistein dapat dioksidasi oleh formaldehida untuk menghasilkan sistein N-formil, yang pemrosesan selanjutnya dapat menyebabkan pembentukan "barang dagangan" (produk kondensasi sistein dengan senyawa aromatik).
Pada hewan, sistein juga digunakan, serta glutamat dan glutamin, untuk sintesis koenzim A, glutathione (GSH), piruvat, sulfat dan asam sulfiderat.
Salah satu metode untuk konversi dari sistein ke piruvat terjadi dalam dua langkah: yang pertama menyiratkan penghapusan atom sulfur dan reaksi transaminasi A kedua.
Ginjal bertanggung jawab atas ekskresi sulfat dan sulfit yang berasal dari metabolisme senyawa sulfur seperti sistein, sementara paru -paru menghembuskan sulfur dioksida dan asam sulfidrik.
Glutathion
Glutathione, molekul yang dibentuk oleh tiga limbah asam amino (glisin, glutamat dan sistein) adalah molekul yang ada pada tanaman, hewan dan bakteri.
Ini memiliki sifat khusus yang menjadikannya "buffer" redoks yang sangat baik, karena melindungi sel dari berbagai jenis stres oksidatif.
Makanan Kaya Sistein
Sistein secara alami ditemukan dalam makanan yang mengandung sulfur sebagai kuning telur (kuning) telur, paprika merah, bawang putih, bawang, brokoli, kembang kol, colliflower, collils dan brussels choles, air dan daun mustard.
Ini juga sebagian besar ada dalam makanan kaya protein seperti daging, kacang -kacangan dan produk susu, di antaranya adalah:
Dapat melayani Anda: ovalbumin: struktur, fungsi, denaturasi- Daging sapi, babi, ayam dan ikan
- Oat dan lentil
- Biji bunga matahari
- Yogurt dan keju
Manfaat asupan sistein
Dianggap bahwa asupannya mencegah kerontokan rambut dan merangsang pertumbuhannya. Dalam industri makanan ini sangat digunakan sebagai agen pijat yang dapat dipanen dan juga untuk "mereproduksi" rasa seperti daging.
Penulis lain telah menekankan bahwa asupan suplemen makanan atau makanan kaya makanan berkurang.
Beberapa suplemen nutrisi yang terkait dengan sistein digunakan oleh manusia sebagai antioksidan, yang dianggap bermanfaat dari sudut pandang "keterlambatan" penuaan.
N-asetil sistein (prekursor dalam sintesis sistein) misalnya, diambil sebagai suplemen nutrisi, karena ini menghasilkan peningkatan biosintesis glutathione (GSH).
Penyakit terkait
Ada beberapa publikasi ilmiah yang menghubungkan tingkat tinggi sistein plasma dengan obesitas dan patologi terkait lainnya seperti penyakit kardiovaskular dan sindrom metabolik lainnya.
Cystinuria, seperti yang disebutkan di atas, adalah patologi yang terkait dengan adanya batu sistin, turunan zip, karena cacat genetik dalam reabsorpsi asam amino dibasic seperti sistin.
Gangguan Kekurangan
Kekurangan sistein telah terkait dengan stres oksidatif, karena ini adalah salah satu prekursor utama untuk sintesis glutathione. Oleh karena itu, kekurangan dalam asam amino ini dapat menyebabkan penuaan dini dan semua flat yang berarti.
Telah ditunjukkan secara eksperimental bahwa suplementasi sistein meningkatkan fungsi otot rangka, mengurangi hubungan antara massa tubuh lemak dan non -lemak, mengurangi kadar plasma sitokin inflamasi, meningkatkan fungsi sistem kekebalan tubuh, dll.
Pada pertengahan tahun 1990 -an, beberapa penelitian menunjukkan bahwa sindrom immunodeficiency (AIDS) yang diperoleh bisa menjadi konsekuensi dari defisiensi sistein yang diinduksi virus.
Pernyataan ini didukung oleh fakta bahwa pasien hi-positif yang diperiksa memiliki kadar sistin dan sistein plasma yang rendah, selain berkurangnya konsentrasi glutathione intraseluler.
Referensi
- Dröge, w. (1993). Defisitas sistein dan glutathione pada pasien AIDS: alasan untuk pengobatan dengan N-seacyl-cysteine. Farmakologi, 46, 61-65.
- Dröge, w. (2005). Stres dan penuaan oksidatif: menua sindrom defisasi sistein? Transaksi Filsafat Masyarakat Kerajaan B: Ilmu Biologi, 360(1464), 2355-2372.
- Elshorbagy, a. K., Smith, a. D., Kozich, v., & Refsum, h. (2011). Sistein dan obesitas. Kegemukan, dua puluh(3), 1-9.
- Kridich, n. (2013). Biosintesis sistein. Ecosal Plus, 1-30.
- McPherson, r. KE., & Hardy, G. (2011). Manfaat klinis dan nutrisi dari suplemen protein yang diperkaya sistein. Pendapat saat ini dalam nutrisi klinis dan perawatan metabolisme, 14, 562-568.
- Mokhtari, v., Afsharian, hlm., Shahhoseini, m., Kalantar, s. M., & Moini, a. (2017). Ulasan tentang berbagai penggunaan n-asetil sistein. Jurnal sel, 19(1), 11-17.
- Piste, hlm. (2013). Antioksidan sistein-master. Jurnal Internasional Ilmu Farmasi, Kimia dan Biologi, 3(1), 143-149.
- Quig, d. (1998). Metabolisme sistein dan toksisitas logam. Ulasan Kedokteran Alternatif, 3(4), 262-270.
- Wu, g. (2013). Asam Aminino. Biokimia dan Nutrisi. Boca Raton, FL: Taylor & Francis Group.
- « Karakteristik Pembelajaran Sosial, Teori Bandura, Contoh
- Dimensi Pendidikan Sosial -Emosional, Pentingnya, Prasekolah »

