Elektroforesis fondasi, teknik, untuk apa, contohnya

- 4134
- 350
- Pete Lesch
Itu Elektroforesis Ini adalah teknik yang digunakan untuk memisahkan molekul dalam medan listrik. Ini harus dilakukan, khususnya, dengan migrasi partikel yang dimuat di bawah pengaruh arus listrik yang diterapkan antara dua kutub, satu positif dan lainnya negatif.
Elektroforesis saat ini merupakan salah satu prosedur paling rutin yang terjadi selama pengembangan percobaan, terutama di bidang yang terkait dengan kimia analitik, biokimia dan ilmu biologis dan medis pada umumnya.
 Bucket Elektroforesis. Sumber: Melodygar/CC BY-SA (https: // CreativeCommons.Org/lisensi/by-sa/4.0)
Bucket Elektroforesis. Sumber: Melodygar/CC BY-SA (https: // CreativeCommons.Org/lisensi/by-sa/4.0) Ini digunakan untuk memisahkan protein, peptida, DNA, RNA dan lainnya sesuai dengan beban, ukuran, kepadatan dan kemurniannya.
Berbagai rumah komersial telah merancang format yang berbeda, dengan aplikasi yang berbeda dan keuntungan yang tepat untuk tujuan tertentu, namun, semua prosedur memerlukan elemen dasar yang sama:
- Sumber energi untuk menghasilkan muatan listrik
- Media dukungan untuk pemisahan
- Solusi buffer (penyangga) Untuk menjaga pH konstan
[TOC]
Dasar
Elektroforesis tidak lebih dari migrasi (pemisahan) partikel atau molekul yang dimuat (secara alami atau artifisial) dalam suatu media atau dukungan di bawah pengaruh medan listrik.
Teknik ini didasarkan pada salah satu persamaan fisik utama elektromagnetisme, yang menurutnya gayanya sama dengan muatan listrik yang dikalikan dengan medan listrik yang diterapkan pada titik itu (F (gaya) = Q (muatan listrik) x E (medan listrik ).
Menurut persamaan ini, dua partikel dengan massa yang sama, tetapi dengan beban yang berbeda, akan bergerak ke laju yang berbeda di medan listrik yang sama. Selain itu, kecepatan pergerakan partikel -partikel ini akan tergantung pada hubungan antara beban dan massa mereka.
Para ilmuwan telah memanfaatkan sifat -sifat ini dan hubungan kargo/massa untuk memisahkan komponen dari biomolekul di bagian terkecil, serta memisahkan molekul yang berbeda dalam campuran, di antara aplikasi lainnya.
Penting untuk diingat bahwa molekul biologis seperti asam amino, peptida, protein, beberapa karbohidrat, nukleotida dan asam nukleat semuanya memiliki sesuatu yang kita sebut "kelompok terionisasi", sehingga mereka dapat ada sebagai spesies positif atau bermuatan negatif dalam kondisi pH tertentu dalam pH tertentu ".
Teknik
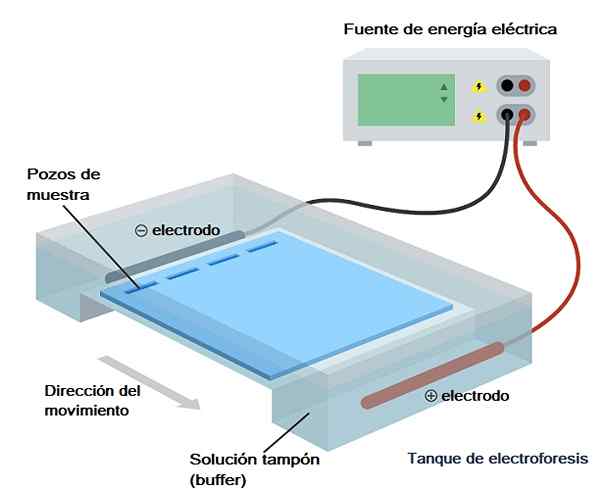
Meskipun ada berbagai jenis elektroforesis, elektroforesis gel adalah yang paling banyak digunakan dalam analisis biokimia, biologi molekuler dan bioteknologi, jadi itu akan menjadi apa yang akan kita bicarakan secara singkat dalam istilah teknis.
Seperti namanya, elektroforesis gel menyiratkan penggunaan media pendukung padat berbentuk padat, baik untuk analisis/pemisahan campuran protein atau asam nukleat (DNA dan/atau RNA) di bawah pengaruh medan listrik listrik.
Sistem atau peralatan yang digunakan untuk melakukan "lari" elektroforetik dapat berupa horizontal (biasanya digunakan untuk asam nukleat) atau vertikal (biasanya digunakan untuk protein).
- Contoh teknik elektroforesis asam nukleat
Asam nukleat biasanya dipisahkan menggunakan gel agarosa (galaktosa polisakarida) yang disiapkan dengan larutan buffer yang memadai (Tris/Acetate/EDTA atau Tris/Borato/EDTA) dan yang konsentrasinya akan menentukan "resolusi" dari fragmen dari berbagai ukuran berbagai ukuran berbagai ukuran yang berbeda ".
Dapat melayani Anda: rantai makanan bumi: tautan dan contohPersiapan sampel
Langkah pertama sebelum melakukan menjalankan elektroforetik dalam gel agarosa adalah untuk mendapatkan sampel. Ini akan tergantung pada ujung eksperimental dan sampel dapat menjadi produk pencernaan enzimatik, pada reaksi berantai polimerase (PCR), pemurnian asam nukleat, dll.
 Campurkan sampel dengan buff beban.Org/lisensi/oleh/4.0) Via Wikimedia Commons)
Campurkan sampel dengan buff beban.Org/lisensi/oleh/4.0) Via Wikimedia Commons) Setelah memperoleh, ini dicampur dengan larutan berwarna (larutan beban) yang memungkinkan pengendapan sampel yang cepat dalam sumur, karena memiliki gliserol dan pewarna yang memungkinkan berjalan secara visual.
Persiapan gel
Langkah ini terdiri dalam mencampur jumlah yang diperlukan dari substrat pembelak -geluk (agarosa) dengan larutan buffer, melelehkannya menggunakan panas dan memperkuatnya pada dukungan yang berfungsi sebagai "cetakan".
Selama Gelifikasi Beberapa "sisir" dimasukkan ke dalam gel yang diposisikan dalam "cetakan" untuk membatasi "sumur" di mana sampel akan diperkenalkan sebelum menjalankan.
Setelah gel didinginkan dan dipadatkan, "sisir" dihapus dan dimasukkan ke dalam wadah yang dikenal sebagai "bucket", yang penuh dengan solusi buffer yang berjalan, (Tris/Acetate/EDTA atau Tris/Borato/Borato/EDTA).
Bucket ini, pada gilirannya, termasuk dalam apa yang disebut "ruang elektroforesis", yang tidak lebih dari wadah yang melaluinya medan listrik dilewatkan dan yang memiliki ruang di mana gel diperkenalkan dan dua bagian yang dipenuhi mereka Solusi penyangga (penyangga berlari).
Kamera ini memiliki dua elektroda, satu positif dan satu negatif, di antaranya gerakan ion diproduksi setelah penerapan medan listrik (terhubung ke sumber daya).
Memuat sampel
Setelah sampel dicampur dengan solusi beban masing -masing, ini dimasukkan ke dalam "sumur" yang sebelumnya dibuat ke dalam gel.
Karena asam nukleat memiliki beban bersih negatif, mereka bermigrasi dari kutub negatif ke yang positif, jadi ini harus diperhitungkan ketika kamera terhubung ke sumber daya, memastikan bahwa kutub negatif sesuai dengan situs sebagian besar di sebelah tempat tersebut dimana sampel dimuat.
Waktu Corrida ditetapkan dalam ketergantungan yang ketat pada peneliti yang bertanggung jawab atas percobaan. Tegangan umumnya dihitung dalam rasio 5 volt per sentimeter dalam gel yang memisahkan dua elektroda.
Menampilkan
Ketika gel berjalan (ketika sampel telah menempuh gel dari satu ujung ke ujung lainnya), itu terendam dalam solusi etid bromida (ETBR), pewarna yang diselingi antara pangkalan nitrogen dan bahwa "merek", jadi " mereka dapat divisualisasikan dalam transilumenant menggunakan lampu ultraviolet.
Untuk apa elektroforesis?
Elektroforesis secara historis telah digunakan dengan berbagai tujuan. Namun, saat ini, kegunaannya sangat tergantung pada "pertanyaan" bahwa peneliti ditanya sehubungan dengan fenomena atau sistem tertentu, serta jenis elektroforesis yang ingin ia gunakan.
Dapat melayani Anda: topoisomerase: apa itu, karakteristik, fungsi, jenisNamun, kita dapat meminta beberapa fungsi utama yang dimiliki teknik ini, dimulai dengan yang paling "langka" dan diakhiri dengan yang paling populer dan sebagian besar dieksploitasi di dunia ilmu biologi. Elektroforesis bermanfaat:
- Untuk analisis kuantitatif campuran kompleks makromolekul dan untuk perhitungan potensi "zeta" (sifat koloid dari suatu partikel dalam media cair di bawah pengaruh medan listrik statis).
- Untuk analisis serum darah untuk tujuan diagnostik.
- Untuk pemisahan glukoprotein, lipoprotein dan hemoglobin darah.
- Untuk analisis makanan, produk farmasi dan polutan lingkungan.
Elektroforesis dalam gel agarosa
- Untuk pemisahan fragmen DNA setelah pencernaan dengan enzim restriksi.
- Untuk pemisahan molekul asam nukleat sebelum dipindahkan ke membran untuk analisis selanjutnya.
- Untuk analisis produk PCR (reaksi berantai polimerase) memverifikasi apakah itu terjadi atau tidak.
- Untuk estimasi ukuran molekul dalam campuran DNA atau RNA.
- Untuk estimasi kuantitas dan/atau kualitas asam nukleat murni.
Elektroforesis dalam gel poliakrilamida dalam kondisi denaturalisasi atau asli
- Untuk menentukan ukuran protein.
- Untuk mengidentifikasi protein.
- Untuk menentukan kemurnian sampel setelah beberapa langkah pemurnian.
- Untuk mengidentifikasi keberadaan tautan disulfida intramolekul.
- Untuk menentukan interaksi antara protein.
- Untuk menentukan titik isoelektrik protein.
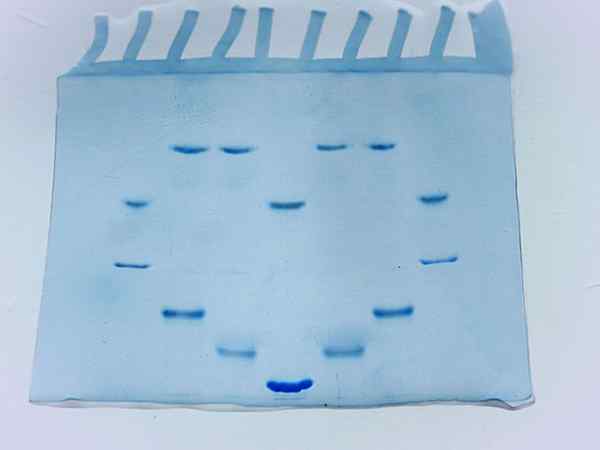 Fotografi gel akrilamida setelah menjalankan beberapa sampel protein (Sumber: Larionova.Marina/cc by-sa (https: // createveCommons.Org/lisensi/by-sa/4.0) Via Wikimedia Commons)
Fotografi gel akrilamida setelah menjalankan beberapa sampel protein (Sumber: Larionova.Marina/cc by-sa (https: // createveCommons.Org/lisensi/by-sa/4.0) Via Wikimedia Commons) Faktor yang mempengaruhi elektroforesis
Migrasi partikel dalam medan listrik tergantung pada berbagai faktor, di antaranya adalah:
- Muatan listrik Anda
- Ukuran molekulnya
- Hidrofobik dan bentuknya
- Besarnya medan listrik yang diterapkan
- Suhu sistem dan gaya ionik dari larutan buffer yang digunakan
- Sifat lingkungan tempat ia berada
Sehubungan dengan sampel
Di antara parameter yang terkait dengan partikel (sampel) yang tunduk pada medan listrik, faktor utama yang mempengaruhi proses ini berkaitan dengan beban, ukuran dan bentuknya.
Semakin besar beban bersih suatu partikel, semakin besar laju migrasinya dan besarnya ini akan tergantung pada pH. Namun, hubungan dengan ukuran berbanding terbalik, yang berarti bahwa semakin "besar" molekul, semakin lambat bermigrasi.
Itu dapat melayani Anda: lia agar (lisin besi): apa itu, fondasi, persiapan, penggunaanSehubungan dengan medan listrik
Sejauh ini kami telah berbicara tentang pentingnya medan listrik untuk mencapai pergerakan partikel dengan elektroforesis, tetapi kami belum menentukan apa itu: gaya listrik per unit beban atau, dalam istilah yang lebih sederhana, suatu wilayah ruang di mana ada gaya listrik.
Parameter tentang medan listrik yang dapat mempengaruhi migrasi adalah tegangan, arus dan resistensi.
Tegangan mempengaruhi "waktu penerbangan" dari molekul yang dipisahkan setelah menerapkan medan listrik. Semakin tinggi, semakin cepat langkah ini.
Arus (elektron kontinu dan seragam yang "didorong" oleh sumber tegangan) dilakukan antara elektroda sistem elektroforetik berkat ion yang ada dalam larutan buffer. Terkait langsung dengan tegangan.
Sehubungan dengan solusi buffer
Komposisi, gaya ionik dan pH larutan buffer adalah parameter utama yang mempengaruhi "lari" elektroforetik, karena mereka secara langsung mempengaruhi beberapa sifat sampel, terutama muatan listrik.
Karena? Larutan buffer menstabilkan pH media dukungan di mana elektroforesis terjadi. Komposisinya dapat mempengaruhi perpindahan partikel migrasi dan konsentrasi ionik juga, karena secara langsung terkait dengan arus.
Sehubungan dengan media dukungan
Berbagai jenis dan format elektroforesis juga menghadirkan media yang berbeda di mana migrasi terjadi dan di mana ia dapat "terdaftar" selanjutnya ".
Laju migrasi molekul yang mengalami elektroforesis tergantung pada jenis media dukungan, yang biasanya harus lembam.
Karakteristik penyerapannya, elektro-osmosis penting (kapasitas pergerakan cairan melalui membran di bawah pengaruh medan listrik) dan kapasitas saringan molekulnya.
Contoh Penggunaan Elektroforesis
Contoh klasik teknik elektroforesis yang digunakan dalam biologi dan bioteknologi meliputi:
- Elektroforesis dalam gel agarosa (bahasa Inggris Gel elektroforesis)
- Elektroforesis dalam gel akrilamida dalam kondisi denaturalisasi (SDS-PAGE, Bahasa Inggris Elektroforesis gel natrium dodecyl sulphat poliacrylamide gel)
- Elektroforesis dalam gel akrilamida dalam kondisi asli (bn-page, bahasa Inggris Elektroforesis gel poliakrilamida asli biru)
- Elektroforesis dalam dua dimensi (2D-halaman, dari bahasa Inggris Elektroforesis gel poliakrilamida dua dimensi)
- Elektroforesis kapiler (dari bahasa Inggris Kapiler elektroforesis)
- Isolectroenfoque (Bahasa Inggris Isolectrophocusing)
- Elektroforesis lapangan berdenyut (bahasa Inggris Elektroforesis lapangan berdenyut)
Referensi
- Beck, Kevin. (2020, 25 Mei). Jenis elektroforesis. Ilmu pengetahuan.com. Diperoleh dari sains.com
- Essays, Inggris. (November 2018). Jenis dan Aplikasi Elektroforesis. Diperoleh dari Ukessays.com
- Nelson, d. L., Lehninger, a. L., & Cox, m. M. (2008). Prinsip -prinsip biokimia lehninger. Macmillan.
- Parmar, hlm. (Agustus 2018). Elektroforesis: Makna, Definisi dan Klasifikasi (dengan Diagram). Teknologi Bio. Diperoleh dari bioteknologi.com
- Perrett, d. (2010). 200 tahun elektroforesis. Chromatog. Hari ini, 4-7.
- Righetti, hlm. G. (2005). Elektroforesis: March of Pennies, March of Dimes. Jurnal Kromatografi A, 1079 (1-2), 24-40.
- Rilbe, h. (sembilan belas sembilan puluh lima). Som mengenang sejarah elektroforesis. Elektroforesis, 16 (1), 1354-1359.
- Vesterberg, atau. (1993). Sejarah singkat metode elektroforesis. Elektroforesis, 14 (1), 1243-1249.
- Vinayagam, m. (Tidak ada tanggal). Faktor -faktor yang mempengaruhi elektroforesis. Akademi.Edu. Diperoleh dari akademisi.Edu
- « Penjelasan Keseimbangan Kimia, Faktor, Jenis, Contoh
- Toltec Culture Origin, Lokasi, Karakteristik, Organisasi »

