Hukum Kedua Rumus Termodinamika, Persamaan, Contoh

- 1592
- 49
- Tommie Smith
Itu Hukum Termodinamika Kedua memiliki beberapa bentuk ekspresi. Salah satunya menyatakan bahwa tidak ada mesin termal yang mampu sepenuhnya mengubah semua energi yang diserap menjadi pekerjaan yang dapat digunakan (formulasi Kelvin-Planck). Cara lain untuk menyatakannya adalah dengan mengatakan bahwa proses nyata terjadi sedemikian rupa sehingga kualitas energi lebih rendah karena Entropi Itu cenderung meningkat.
Undang -undang ini, juga dikenal sebagai prinsip kedua termodinamika, telah dinyatakan dengan cara yang berbeda dengan berlalunya waktu, dari awal abad ke -19 hingga saat ini, meskipun asal -usulnya berasal dari penciptaan mesin uap pertama di Inggris, Di awal abad ke -18.
 Gambar 1. Saat membangun blok konstruksi ke lantai, akan sangat mengejutkan untuk jatuh dipesan. Sumber: Pixabay.
Gambar 1. Saat membangun blok konstruksi ke lantai, akan sangat mengejutkan untuk jatuh dipesan. Sumber: Pixabay. Tetapi meskipun diekspresikan dalam banyak hal, dalam semua gagasan bahwa materi cenderung gangguan dan bahwa tidak ada proses 100%, karena kerugian akan selalu ada akan selalu ada.
Semua sistem termodinamika mematuhi prinsip ini, dimulai dengan alam semesta itu sendiri ke secangkir kopi pagi yang menunggu dengan tenang di atas meja bertukar panas dengan lingkungan.
Kopi mendingin seiring berjalannya waktu, sampai berada dalam keseimbangan termal dengan lingkungan, jadi akan sangat mengejutkan jika suatu hari yang sebaliknya akan terjadi dan atmosfer akan dingin saat kopi akan memanas untuk dirinya sendiri. Tidak mungkin terjadi, beberapa orang akan mengatakan itu tidak mungkin, tetapi sudah cukup untuk membayangkan memiliki gagasan tentang perasaan di mana hal -hal terjadi secara spontan.
Dalam contoh lain, jika kita menggeser buku di permukaan meja, pada akhirnya akan berhenti, karena energi kinetiknya akan hilang dalam bentuk panas karena gesekan.
Hukum termodinamika pertama dan kedua didirikan sekitar tahun 1850, terima kasih kepada para ilmuwan seperti Lord Kelvin -creator dari istilah "termodinamika" -, William Rankine -penulis teks formal pertama dari termodinamika -dan Rudolph Clausius.
[TOC]
Rumus dan Persamaan
Entropy -less dari awal -membantu kita menetapkan pengertian di mana hal -hal terjadi. Mari kita kembali ke contoh tubuh dalam kontak termal.
Ketika dua objek pada suhu yang berbeda dihubungi dan akhirnya setelah beberapa saat mereka mencapai keseimbangan termal, mereka didorong ke sana oleh fakta bahwa entropi mencapai maksimum, ketika suhu keduanya sama adalah sama adalah sama.
Menunjukkan entropi sebagai S, Perubahan entropi ΔS suatu sistem diberikan oleh:

Perubahan entropi ΔS Ini menunjukkan tingkat gangguan dalam suatu sistem, tetapi ada pembatasan dalam penggunaan persamaan ini: ini hanya berlaku untuk proses yang dapat dibalik, yaitu, di mana sistem dapat kembali ke keadaan aslinya tanpa meninggalkan tanda apa yang akan telah terjadi-.
Dalam proses yang tidak dapat diubah, hukum kedua termodinamika dimanifestasikan sebagai berikut:
Dapat melayani Anda: Nomor Reynolds: Untuk apa itu, bagaimana itu dihitung, latihan
Proses reversibel dan tidak dapat diubah
Cangkir kopi selalu dingin dan merupakan contoh yang baik dari proses yang tidak dapat diubah, karena selalu terjadi dalam satu arah. Jika krim ditambahkan ke kopi dan aduk, kombinasi yang sangat menyenangkan akan diperoleh, tetapi tidak peduli bagaimana aduk lagi, kopi dan krim tidak akan lagi, karena aduk tidak dapat diubah.
 Gambar 2. Kerusakan cangkir adalah proses yang tidak dapat diubah. Sumber: Pixabay.
Gambar 2. Kerusakan cangkir adalah proses yang tidak dapat diubah. Sumber: Pixabay. Meskipun sebagian besar proses sehari -hari tidak dapat diubah, beberapa hampir Reversibel. Reversibilitas adalah idealisasi. Untuk dilakukan, sistem harus berubah sangat lambat, sehingga pada setiap titik itu selalu seimbang. Dengan cara ini dimungkinkan untuk mengembalikannya ke negara bagian sebelumnya tanpa meninggalkan tanda sekitar.
Proses yang cukup dekat dengan cita -cita ini lebih efisien, karena mereka memberikan jumlah pekerjaan yang lebih besar dengan konsumsi energi yang lebih sedikit.
Kekuatan gesekan bertanggung jawab atas sebagian besar ireversibilitas, karena panas yang dihasilkan olehnya bukanlah jenis energi yang dicari. Dalam buku yang meluncur di atas meja, panas dengan gesekan adalah energi yang tidak dipulihkan.
Meskipun buku ini kembali ke posisi semula, meja akan menjadi panas sebagai jejak kaki datang dan melanjutkannya.
Sekarang amati bohlam pijar: sebagian besar pekerjaan yang dilakukan oleh arus yang melintasi filamen terbuang dalam panas oleh efek joule. Hanya sebagian kecil yang digunakan untuk memancarkan cahaya. Dalam kedua proses (buku dan bohlam), entropi sistem telah meningkat.
Aplikasi
Mesin yang ideal adalah yang dibangun melalui proses reversibel dan tidak memiliki gesekan yang menyebabkan limbah energi, berbelok hampir Semua energi termal dalam pekerjaan yang dapat digunakan.
Kami hampir menekankan kata itu, karena bahkan mesin yang ideal, yang merupakan carnot, memiliki efisiensi 100%. Hukum termodinamika kedua tidak dengan cara ini.
Mesin Carnot
Mesin Carnot adalah mesin paling efisien yang dapat dirancang. Ini beroperasi antara dua endapan suhu dalam dua proses isotermal - pada suhu konstan - dan dua proses adiabatik - tanpa transfer energi termal-.
Grafik yang disebut diagram tekanan PV - volume- Klarifikasi situasinya:
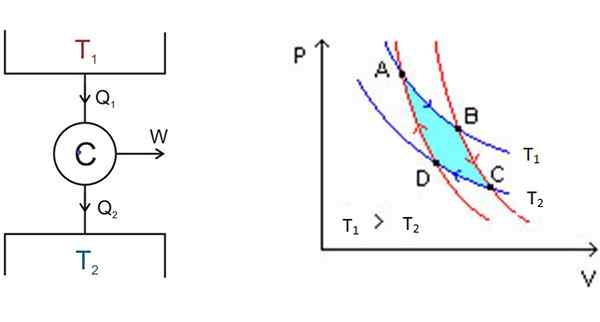 Gambar 3. Di sebelah kiri Skema Mesin Carnot dan di sebelah kanan diagram P-V. Sumber: Wikimedia Commons.
Gambar 3. Di sebelah kiri Skema Mesin Carnot dan di sebelah kanan diagram P-V. Sumber: Wikimedia Commons. Di sebelah kiri, pada Gambar 3 adalah skema motor Carnot C, yang mengambil panas q1 deposit pada suhu t1, mengubah panas itu menjadi pekerjaan dan memberi buang itu2 ke deposit terdingin, yaitu pada suhu t2.
Mulai dari A, sistem mengembang sampai mencapai B, menyerap panas ke suhu tetap t1. Di B, sistem memulai ekspansi adiabatik di mana panas tidak dimenangkan atau hilang, untuk mencapai c.
Di C dimulai proses isotermal lain: untuk memberikan panas pada deposit termal lebih dingin lainnya yang ada di T2. Karena ini terjadi sistem dikompresi dan titik D tercapai. Di sana dimulai proses adiabatik kedua untuk kembali ke titik awal. Dengan cara ini siklus selesai.
Itu dapat melayani Anda: perpindahan panas dengan mengemudi (dengan contoh)Efisiensi Carnot tergantung pada suhu di Kelvin pada dua deposit termal:
Efisiensi maksimum = (qpintu masuk - QKELUAR) /Qpintu masuk = 1 - (t2/T1)
Teorema Carnot menyatakan bahwa ini adalah mesin termal yang paling efisien, tetapi jangan terburu -buru untuk membelinya. Apakah Anda ingat apa yang kami katakan tentang reversibilitas proses? Mereka harus terjadi dengan sangat, sangat lambat, sehingga daya output mesin ini praktis nol.
Metabolisme manusia
Manusia membutuhkan energi untuk menjaga semua sistem mereka berfungsi, oleh karena itu mereka berperilaku sebagai mesin termal yang menerima energi dan mengubahnya menjadi energi mekanik menjadi, misalnya, bergerak.
Efisiensi Dan dari tubuh manusia saat melakukan pekerjaan dapat didefinisikan sebagai rasio antara kekuatan mekanik yang dapat disediakannya dan entri energi total, yang dilengkapi dengan makanan.
Seperti kekuatan rata -rata pM Itu adalah pekerjaan yang dilakukan dalam interval waktu Δt, Itu bisa dinyatakan sebagai:
PM = W/Δt
Ya ΔU/Δt Ini adalah laju energi yang ditambahkan, efisiensi tubuh tetap:

Melalui banyak tes dengan sukarelawan, efisiensi hingga 17%telah diperoleh, menghasilkan sekitar 100 watt daya selama beberapa jam.
Tentu saja, ini akan sangat tergantung pada tugas yang dilakukan. Mengayuh sepeda memiliki efisiensi yang sedikit lebih besar, sekitar 19 %, sedangkan tugas berulang yang meliputi bilah, puncak dan cangkul memiliki efisiensi serendah sekitar 3 %.
Contoh
Hukum termodinamika kedua tersirat dalam semua proses yang terjadi di alam semesta. Entropi selalu tumbuh, meskipun dalam beberapa sistem tampaknya berkurang. Untuk ini meningkat di tempat lain, sehingga dalam keseimbangan total itu positif.
- Dalam belajar ada entropi. Ada orang yang belajar hal -hal dengan baik dan cepat, selain bisa mengingatnya dengan mudah. Dikatakan bahwa mereka adalah orang -orang dengan pembelajaran entropi rendah, tetapi mereka pasti kurang banyak daripada entropi tinggi: mereka yang paling ingat hal -hal yang mereka pelajari.
- Perusahaan dengan pekerja yang tidak terorganisir memiliki lebih banyak entropi daripada yang ada di mana pekerja melakukan tugas dengan cara yang tertib. Jelas bahwa yang terakhir akan lebih efisien daripada yang pertama.
- Kekuatan gesekan menghasilkan lebih sedikit efisiensi dalam fungsi mesin, karena mereka meningkatkan jumlah energi yang hilang yang tidak dapat digunakan secara efisien.
- Meluncurkan dadu memiliki entropi yang lebih besar daripada melemparkan koin ke udara. Lagi pula, meluncurkan mata uang hanya memiliki 2 hasil yang mungkin, saat meluncurkan dadu adalah 6. Semakin banyak peristiwa yang mungkin, semakin banyak entropi.
Dapat melayani Anda: apa elemen gerakan?Latihan terpecahkan
Latihan 1
Silinder dengan piston diisi dengan campuran uap cairan dan air pada 300 K dan 750 kJ panas ditransfer ke proses tekanan konstan. Akibatnya, cairan di dalam silinder diuapkan. Hitung perubahan entropi dalam proses.
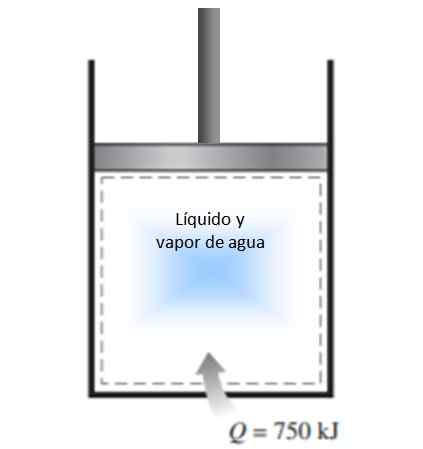 Gambar 4. Gambar untuk contoh diselesaikan 1. Sumber: f. Zapata.
Gambar 4. Gambar untuk contoh diselesaikan 1. Sumber: f. Zapata. Larutan
Proses yang dijelaskan dalam pernyataan dilakukan pada tekanan konstan dalam sistem tertutup, yang tidak mengalami pertukaran massal.
Karena penguapan, selama suhu tidak berubah (selama fase berubah suhu konstan), definisi perubahan entropi yang diberikan di atas dapat diterapkan dan suhu dapat meninggalkan integral:

ΔS = 750.000 J / 300 K = 2500 J / k.
Karena sistem datang ke sistem, perubahan entropi positif.
Latihan 2
Gas mengalami peningkatan tekanan 2.00 hingga 6.00 Atmospheres (ATM), mempertahankan volume konstan 1.00 m3, dan kemudian berkembang dengan tekanan konstan sampai mencapai volume 3.00 m3. Akhirnya kembali ke keadaan awalnya. Hitung berapa banyak pekerjaan yang dilakukan dalam 1 siklus.
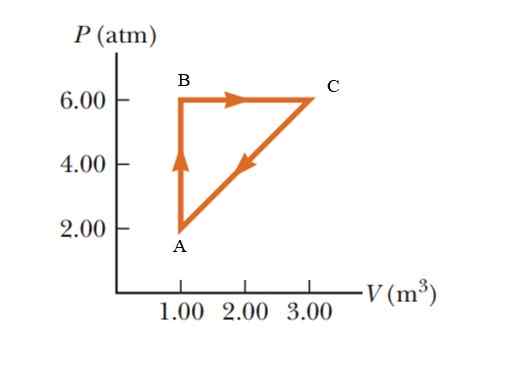 Gambar 5. Proses termodinamika dalam gas misalnya 2. Sumber: Serway -Vulle. Dasar -dasar fisika.
Gambar 5. Proses termodinamika dalam gas misalnya 2. Sumber: Serway -Vulle. Dasar -dasar fisika. Larutan
Ini adalah proses siklik di mana variasi energi internal batal, menurut hukum termodinamika pertama, oleh karena itu q = w. Dalam diagram p -V (tekanan - volume), pekerjaan yang dilakukan selama proses siklus setara dengan area yang dikunci oleh kurva. Untuk memberikan hasil dalam sistem internasional, perlu untuk mengubah unit dalam tekanan melalui faktor konversi berikut:
1 atm = 101.325 kPa = 101.325 pa.
Area yang terlampir oleh grafik sesuai dengan segitiga yang alasnya (3 - 1 m3) = 2 m3 dan tingginya (6 - 2 atm) = 4 atm = 405.300 Pa
WABCA = ½ (2 m3 x 405300 pa) = 405300 j = 405.3 kJ.
Latihan 3
Dikatakan bahwa salah satu mesin paling efisien yang telah dibangun adalah turbin uap yang dipicu oleh batubara di Sungai Ohio, yang digunakan untuk menggerakkan generator listrik yang beroperasi antara tahun 1870 dan 430 ° C.
Hitung: a) Efisiensi teoritis maksimum, b) Daya mekanik yang dikirim oleh mesin jika diserap 1.40 x 105 J energi setiap detik dari tangki panas. Diketahui bahwa efisiensi nyata adalah 42.0%.
Larutan
a) Efisiensi maksimum dihitung dengan persamaan yang diberikan di atas:
Efisiensi maksimum = (qpintu masuk - Q KELUAR) /Qpintu masuk = 1 - (t2/T1)
Untuk meneruskan Celsius ke Kelvin, itu cukup untuk menambahkan 273.15 pada suhu Celcius:
Mengalikan 100% Anda memiliki efisiensi persentase maksimum, yaitu 67.2%
c) Jika efisiensi sebenarnya adalah 42%, ada efisiensi maksimum 0.42.
Daya mekanik yang disampaikan adalah: p = 0.42 x 1.40 x10 5 J/s = 58800 w.
Referensi
- Bauer, w. 2011. Fisika untuk Teknik dan Ilmu Pengetahuan. Volume 1. MC Graw Hill.
- Cengel, dan. 2012. Termodinamika. 7ma Edisi. Bukit McGraw.
- Figueroa, d. (2005). Seri: Fisika untuk Sains dan Teknik. Volume 4. Cairan dan termodinamika. Diedit oleh Douglas Figueroa (USB).
- Knight, r. 2017. Fisika untuk Ilmuwan dan Teknik: Pendekatan Strategi.
- López, c. Hukum Termodinamika Pertama. Dipulihkan dari: CulturAcientifica.com.
- Serway, r. 2011. Dasar -dasar fisika. 9na Pembelajaran Cengage.
- Universitas Sevilla. Mesin termal. Pulih dari: Laplace.kita.adalah
- « Prinsip -prinsip Teori Pengacara, Periode dan Pola
- Perubahan jenis negara dan karakteristiknya (dengan contoh) »


=0.672)